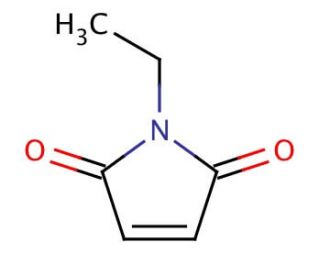
N-Ethylmaleimide (CAS 128-53-0)
Produktreferenzen ansehen (19)
Direktverknüpfungen
N-Ethylmaleimid (NEM) ist eine elektrophile kleine Molekül, das in der biologischen Forschung verwendet wird, um nucleophile Thiolreste an Proteinen alkylieren und kovalent modifizieren zu können. Die kovalente Modifizierung des aktiven Thiolrests von Cystein-Proteasen unterbindet die Funktion des Enzyms. N-Ethylmaleimid zeigt auch eine Hemmung der Mg2+-abhängigen internukleosomalen DNA-Fragmentierung, ein definierendes Ereignis des apoptotischen Pfades. Andere thiophile Spezies wie Hg2+ und Cd2+ hemmen ebenfalls die Fragmentierung, was darauf hindeutet, dass eine Thiolgruppe für diese Degradation notwendig ist. Die NADP-abhängige Isocitrat-Dehydrogenase in Hefe wird durch N-Ethylmaleimid deaktiviert, was auf eine Alkylierung eines Cysteinrests gefolgt von einer langsameren Alkylierung eines Lysinrests auf dem Enzym hindeutet. N-Ethylmaleimid ist auch ein Aktivator von PLA2.
N-Ethylmaleimide (CAS 128-53-0) Literaturhinweise
- Die mitochondriale akzessorische Untereinheit p55 der menschlichen DNA-Polymerase gamma verstärkt die DNA-Bindung, fördert die prozessive DNA-Synthese und verleiht N-Ethylmaleimid-Resistenz. | Lim, SE., et al. 1999. J Biol Chem. 274: 38197-203. PMID: 10608893
- N-Ethylmaleimid hemmt die durch den Plättchenwachstumsfaktor BB stimulierte Akt-Phosphorylierung über die Aktivierung der Proteinphosphatase 2A. | Yellaturu, CR., et al. 2002. J Biol Chem. 277: 40148-55. PMID: 12171932
- Hemmung des KCl-Kotransports durch Okadasäure. Nachweis, dass die Dephosphorylierung von Proteinen für die Aktivierung des Transports durch Zellschwellung oder N-Ethylmaleimid notwendig ist. | Jennings, ML. and Schulz, RK. 1991. J Gen Physiol. 97: 799-817. PMID: 1647439
- Nachweis von Glutathion in Vollblut nach Stabilisierung mit N-Ethylmaleimid. | Giustarini, D., et al. 2011. Anal Biochem. 415: 81-3. PMID: 21545786
- Analyse von GSH und GSSG nach Derivatisierung mit N-Ethylmaleimid. | Giustarini, D., et al. 2013. Nat Protoc. 8: 1660-9. PMID: 23928499
- Reinigung eines N-Ethylmaleimid-empfindlichen Proteins, das den vesikulären Transport katalysiert. | Block, MR., et al. 1988. Proc Natl Acad Sci U S A. 85: 7852-6. PMID: 3186695
- Intramitochondriale Phospholipase-Aktivität und die Auswirkungen von Ca2+ und N-Ethylmaleimid auf die mitochondriale Funktion. | Pfeiffer, DR., et al. 1979. J Biol Chem. 254: 11485-94. PMID: 40983
- Die Modulation von Ca2+-Kanälen durch PTX-empfindliche G-Proteine wird durch N-Ethylmaleimid in sympathischen Neuronen der Ratte blockiert. | Shapiro, MS., et al. 1994. J Neurosci. 14: 7109-16. PMID: 7525895
- Die DNA-Spaltung in Rattenleberkernen, die durch Mg2+ oder Ca2+ + Mg2+ aktiviert werden, wird durch eine Reihe strukturell nicht verwandter Inhibitoren gehemmt. | Cain, K., et al. 1994. Biochem Cell Biol. 72: 631-8. PMID: 7654337
- N-Ethylmaleimid-Profilierung der NADP-abhängigen Isocitrat-Dehydrogenase der Hefe. | Huang, YC., et al. 1995. Arch Biochem Biophys. 316: 485-92. PMID: 7840654
- N-Ethylmaleimid stimuliert die Freisetzung von Arachidonsäure durch Aktivierung der signalabhängigen Phospholipase A2 in Endothelzellen. | Neve, EP., et al. 1995. Biochem Pharmacol. 49: 57-63. PMID: 7840783
- Die mehrstufige DNA-Spaltung in Rattenleberkernen wird durch reaktive Thiolverbindungen gehemmt. | Cain, K., et al. 1995. FEBS Lett. 358: 255-61. PMID: 7843412
- Strukturelle Merkmale, die die Faltung homologer Proteine in zellfreien Translationssystemen steuern. Die Wirkung einer auf Mitochondrien ausgerichteten Presequenz auf Aspartat-Aminotransferase. | Mattingly, JR., et al. 1993. J Biol Chem. 268: 26320-7. PMID: 8253754
- Die Charakterisierung von Glutathion-S-Transferasen aus dem Riechepithel der Ratte. | Banger, KK., et al. 1993. Biochem J. 290 (Pt 1): 199-204. PMID: 8439289
- Bestimmung von Schwefelwasserstoff mit 5,5'-Dithiobis-(2-nitrobenzoesäure), N-Ethylmaleimid und Parachlormercuribenzoat. | Nashef, AS., et al. 1977. Anal Biochem. 79: 394-405. PMID: 869184
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
N-Ethylmaleimide, 1 g | sc-202719A | 1 g | $22.00 | |||
N-Ethylmaleimide, 5 g | sc-202719 | 5 g | $68.00 | |||
N-Ethylmaleimide, 25 g | sc-202719B | 25 g | $210.00 | |||
N-Ethylmaleimide, 100 g | sc-202719C | 100 g | $780.00 | |||
N-Ethylmaleimide, 250 g | sc-202719D | 250 g | $1880.00 |
