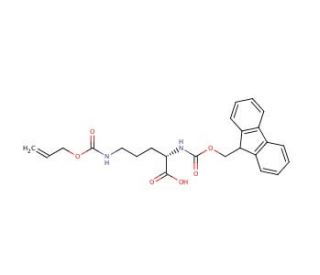
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7)
QUICK LINKS
Fmoc-Orn(Alloc)-OH represents a derivative of the amino acid Ornithine, which occurs naturally and participates in nitrogen metabolism as an intermediate in the urea cycle. Widely employed in organic synthesis and biochemistry, this amino acid derivative holds significant versatility. It serves multiple purposes, including protein and peptide synthesis, as well as serving as a starting material for the synthesis of various compounds. In scientific research, Fmoc-Orn(Alloc)-OH finds extensive applications, particularly in peptide synthesis and protein synthesis. Its usefulness lies in the introduction of diverse functional groups into peptides and proteins. Moreover, this compound is utilized in synthesizing other compounds like small molecules and polymers. Its capability to introduce a wide range of functional groups into these compounds is highly advantageous. The mechanism of action for Fmoc-Orn(Alloc)-OH hinges upon its reactivity with amino acids and other molecules. Through its interaction with an amino acid, it forms a covalent bond known as a peptide bond, facilitating the linking of amino acids to create peptides and proteins. Furthermore, Fmoc-Orn(Alloc)-OH can establish covalent bonds with small molecules and polymers through its reactions with them.
Fmoc-Orn(Alloc)-OH (CAS 147290-11-7) References
- Synthesis of and specific antibody generation for glycopeptides with arginine N-GlcNAcylation. | Pan, M., et al. 2014. Angew Chem Int Ed Engl. 53: 14517-21. PMID: 25353391
- Specific tandem mass spectrometric detection of AGE-modified arginine residues in peptides. | Schmidt, R., et al. 2015. J Mass Spectrom. 50: 613-24. PMID: 25800199
- Selective sensing of pyrophosphate in physiological media using zinc(II)dipicolylamino-functionalised peptides. | Zwicker, VE., et al. 2015. Org Biomol Chem. 13: 7822-9. PMID: 26107804
- Synthetic peptides mimicking the binding site of human acetylcholinesterase for its inhibitor fasciculin 2. | Kafurke, U., et al. 2015. J Pept Sci. 21: 723-30. PMID: 26200472
- Resolving the α-glycosidic linkage of arginine-rhamnosylated translation elongation factor P triggers generation of the first ArgRha specific antibody. | Li, X., et al. 2016. Chem Sci. 7: 6995-7001. PMID: 28451135
- Recognition of Dimethylarginine Analogues by Tandem Tudor Domain Protein Spindlin1. | Porzberg, MRB., et al. 2022. Molecules. 27: PMID: 35164245
- Biocompatible and Selective Generation of Bicyclic Peptides. | Ullrich, S., et al. 2022. Angew Chem Int Ed Engl. 61: e202208400. PMID: 35852030
- Pegylated peptides. II. Solid-phase synthesis of amino-, carboxy- and side-chain pegylated peptides. | Lu, YA. and Felix, AM. 1994. Int J Pept Protein Res. 43: 127-38. PMID: 8200730
- A dual role of phenylboronic acid as a receptor for carbohydrates as well as a quencher for neighboring pyrene fluorophore | Lok Nath Neupane, Chuda Raj Lohani, Jeongho Kim, Keun-Hyeung Lee. 2013. Tetrahedron. 69: 11057-11063.
- Total synthesis of TRADD death domain with arginine N-GlcNAcylation by hydrazide-based native chemical ligation | Ye Wu a b 1, Yulei Li c 1, Wei Cong a, Yan Zou b, Xiang Li b, Honggang Hu a. 2020. Chinese Chemical Letters. 31: 107-110.
Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
Fmoc-Orn(Alloc)-OH, 5 g | sc-235198 | 5 g | $156.00 |
