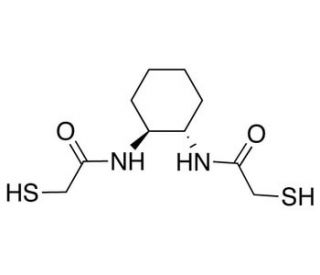
Structure moléculaire de (+/-)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane, Numéro CAS: 257641-01-3
(±)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane (CAS 257641-01-3)
Noms alternatifs:
Vectrase P; 2-sulfanyl-N-[2-[(2-sulfanylacetyl)amino]cyclohexyl]acetamide
Application(s):
(+/-)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane est un agent utile de repliement des protéines contenant du disulfure
Numéro CAS:
257641-01-3
Pureté:
98%
Masse Moléculaire:
262.39
Formule Moléculaire:
C10H18N2O2S2
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le (+/-)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane est un composé de cyclohexane substitué par deux groupes mercaptoacetamido. Le (+/-)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane a été décrit pour accélérer efficacement le repliement oxydatif des protéines par interaction avec les réactions d'échange thiol-disulfure, et il a été démontré qu'il était particulièrement efficace pour le repliement des protéines contenant des disulfures.
(±)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane (CAS 257641-01-3) Références
- Une petite molécule catalyseur du repliement des protéines in vitro et in vivo. | Woycechowsky, KJ., et al. 1999. Chem Biol. 6: 871-9. PMID: 10631515
- Effets du pKa des thiols aromatiques sur le taux de repliement d'une protéine contenant des disulfures. | Gough, JD., et al. 2003. Biochemistry. 42: 11787-97. PMID: 14529290
- Investigation du repliement des protéines à l'aide d'un écran factoriel fractionné: étude des effets et des interactions des réactifs. | Willis, MS., et al. 2005. Protein Sci. 14: 1818-26. PMID: 15937284
- Déterminants structuraux de l'accès au substrat de la disulfure oxydase Erv2p. | Vala, A., et al. 2005. J Mol Biol. 354: 952-66. PMID: 16288914
- Les petites molécules non réactives à l'oxydation peuvent accélérer le repliement oxydatif des protéines par de nouveaux mécanismes. | Fink, M., et al. 2008. Biophys Chem. 132: 104-9. PMID: 18045767
- Catalyseurs à petites molécules du repliement oxydatif des protéines. | Lees, WJ. 2008. Curr Opin Chem Biol. 12: 740-5. PMID: 18824127
- Les disélénides à petites molécules catalysent le repliement oxydatif des protéines in vivo. | Beld, J., et al. 2010. ACS Chem Biol. 5: 177-82. PMID: 20052969
- Optimisation des méthodes de pliage oxydatif pour les peptides riches en cystéine: étude des conotoxines contenant trois ponts disulfures. | Steiner, AM. and Bulaj, G. 2011. J Pept Sci. 17: 1-7. PMID: 20814907
- Acyl cystamine: imitations de petites foldases moléculaires accélérant le repliement oxydatif de protéines contenant des disulfures. | Wang, GZ., et al. 2011. Biotechnol Prog. 27: 377-85. PMID: 21302368
- Efficacité de l'acide nucléique peptidique et de conjugués sélectionnés contre des pathologies cellulaires spécifiques de la sclérose latérale amyotrophique. | Browne, EC., et al. 2016. Bioorg Med Chem. 24: 1520-7. PMID: 26935939
- L'activité redox de la protéine disulfure isomérase inhibe les phénotypes de la SLA dans des modèles cellulaires et de poisson zèbre. | Parakh, S., et al. 2020. iScience. 23: 101097. PMID: 32446203
- Les disulfures peptidiques CGC et RKCGC facilitent le repliement oxydatif des protéines | Guo-Zhen Wang, Xiaoyan Dong, Yan Sun. 2011. Biochemical Engineering Journal. Volume 55, Issue 3: 169-175.
- Le disulfure peptidique RKCGCFF facilite le repliement oxydatif des protéines en imitant la protéine disulfure isomérase | Hu Liu, Xiao-Yan Dong, Yan Sun. 2013. Biochemical Engineering Journal. 79: 29-32.
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
(±)-trans-1,2-Bis(2-mercaptoacetamido)cyclohexane, 100 mg | sc-213078 | 100 mg | $379.00 |
