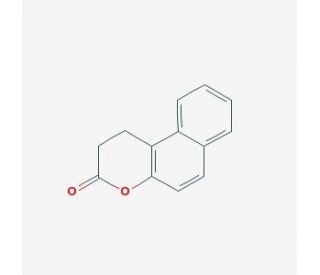
Splitomicin 의 분자 구조, CAS 번호: 5690-03-9
Splitomicin (CAS 5690-03-9)
대체 이름:
1,2-Dihydro-3H-naphtho[2,1-b]pyran-3-one; 1-Naphthalen propanoic acid
적용:
Splitomicin 는 Sir2p 히스톤 탈활성화 억제제입니다.
CAS 등록번호:
5690-03-9
순도:
≥98%
분자량:
198.22
분자식:
C13H10O2
연구용으로만 사용가능합니다. 진단이나 치료용으로 사용불가합니다.
* 참조분석증명서대량의 측정 데이터(함수량포함).
빠른 링크
주문정보
설명
기술정보
안전정보
SDS 및 분석 증명서
과학 연구에서 관심의 대상이 되고 있는 화합물인 스플리토미닌은 주로 효소 시르투인 2(SIRT2)의 특정 억제제로서의 역할에 대해 연구되어 왔습니다. 이 화합물의 작용 메커니즘은 SIRT2의 촉매 부위에 결합하여 탈아세틸화 효소 활성을 억제하는 것입니다. SIRT2는 유전자 발현, 신진대사, 스트레스 반응 등 다양한 세포 과정을 조절하는 데 중요한 역할을 하는 NAD+ 의존성 단백질 탈아세틸화 효소인 시르투인 계열에 속합니다. 스플리토마이신을 활용한 연구는 SIRT2의 기능과 세포 생리 및 병리와의 관련성에 대한 통찰력을 제공했습니다. 세포 주기 진행, 세포 골격 역학 및 자가포식과 같은 세포 과정에 대한 SIRT2 억제의 영향을 조사하기 위해 스플리토마이신을 사용한 연구들이 진행되었습니다. 또한 암, 신경 퇴행성 질환, 대사 증후군과 같은 질병에서 SIRT2를 표적으로 삼을 수 있는 가능성을 탐색하기 위해 실험 모델에서 스플리토마이신을 활용하고 있습니다. 또한, 스플리토미닌은 시르투인 매개 신호 전달 경로의 기초가 되는 분자 메커니즘을 분석하고 약리학적인 개입을 위한 잠재적 표적을 식별하는 데 유용한 도구로 사용됩니다. 전반적으로 스플리토미닌은 건강과 질병에서 시르투인의 역할을 설명할 수 있는 기회를 제공하는 생물의학 연구의 중요한 자산입니다.
Splitomicin (CAS 5690-03-9) 참고자료
- Sir2p의 저분자 억제제 확인. | Bedalov, A., et al. 2001. Proc Natl Acad Sci U S A. 98: 15113-8. PMID: 11752457
- 효모에서 표현형 스크린을 사용하여 NAD+ 의존성 탈아세틸화 효소의 선택적 억제제를 확인합니다. | Hirao, M., et al. 2003. J Biol Chem. 278: 52773-82. PMID: 14534292
- 피다레스타트는 히스톤 탈아세틸화 효소 Sir2 의존적 메커니즘을 통해 db/db 당뇨병성 비만 마우스의 심근세포 수축 기능을 개선합니다. | Dong, F. and Ren, J. 2007. J Hypertens. 25: 2138-47. PMID: 17885559
- 시르투인 저해제로서 스플리토마이신 유도체에 대한 구조-활성 연구 및 결합 모드의 전산 예측. | Neugebauer, RC., et al. 2008. J Med Chem. 51: 1203-13. PMID: 18269226
- 스플리토마이신은 순환 AMP 포스포디에스테라아제 및 세포 내 Ca++ 방출 억제를 통해 인간 혈소판 응집을 억제합니다. | Liu, FC., et al. 2009. Thromb Res. 124: 199-207. PMID: 19327818
- 스플리토마이신은 ERK 경로의 cAMP/PKA 신호 억제를 활성화하여 인간 호중구에서 fMLP에 의한 슈퍼옥사이드 음이온 생성을 억제합니다. | Liu, FC., et al. 2012. Eur J Pharmacol. 688: 68-75. PMID: 22634165
- 시르투인 활성화제 및 억제제. | Villalba, JM. and Alcaín, FJ. 2012. Biofactors. 38: 349-59. PMID: 22730114
- 산화 스트레스 하에서 SIRT1 조절제에 의한 FOXO 및 p53의 조절. | Hori, YS., et al. 2013. PLoS One. 8: e73875. PMID: 24040102
- SIRT1 억제제인 스플리토마이신은 마우스 배아 줄기세포의 조혈 분화를 향상시킵니다. | Park, JA., et al. 2019. Int J Stem Cells. 12: 21-30. PMID: 30836727
- 님볼리드는 시르투인 의존적으로 β-카테닌/Smad를 조절하여 세룰린으로 유발된 만성 췌장염을 제거합니다. | Bansod, S., et al. 2020. Pharmacol Res. 156: 104756. PMID: 32194177
의 억제제:
A530032D15Rik, Ataxin-7, Enzyme, HDAC, HIRA, IGFL1, NAT-11, NAT-13, SENP (SUMO specific peptidase), Sir2, Sir3, SIRT1, SIRT4, SIRT7, SMRT/SMRTe, SUT-1.의 활성화자:
Sir4.주문정보
| 제품명 | 카탈로그 번호 | 단위 | 가격 | 수량 | 관심품목 | |
Splitomicin, 5 mg | sc-358701 | 5 mg | $48.00 |
