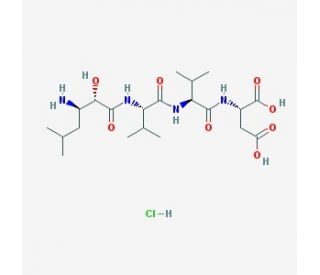
Amastatin hydrochloride (CAS 100938-10-1)
See product citations (3)
QUICK LINKS
Amastatin hydrochloride is a slow, tightly binding, competitive inhibitor of human serum aminopeptidase A, human serum aminopeptidase M (CD13), pig kidney leucine aminopeptidase (LAP3), and tyrosine aminopeptidase, but not of aminopeptidase B. The compound has been used to potentiate the action of some bioactive peptides by inhibiting their degradation by aminopeptidases. Amastatin hydrochloride may act to slightly decrease the conversion of angiontensin II to angiotensin III, but significantly increases the potency of angiotensin III and des(Asp1)angiotensin I. In addition, the Suc-Ala-Ala-Pro-Leu-pNA amidolytic enzyme activities were completely inhibited with the addition of amastatin hydrochloride.
Amastatin hydrochloride (CAS 100938-10-1) References
- Inhibitors on an elastase-like enzyme activity catalyzing Suc-Ala-Ala-Pro-Leu-pNA amidolysis in human seminal plasma. | Matsuda, Y., et al. 2000. Arch Androl. 44: 1-9. PMID: 10690759
- Localization of carboxypeptidase A-like enzyme in rat kidney. | Igić, R., et al. 2003. Peptides. 24: 1237-40. PMID: 14612196
- Purification and characterization of aminopeptidase N from Spodoptera litura expressed in Sf21 insect cells. | Kaur, R., et al. 2007. Protein Expr Purif. 54: 267-74. PMID: 17467291
- Role of aminopeptidase activity in the regulation of the pressor activity of circulating angiotensins. | Ahmad, S. and Ward, PE. 1990. J Pharmacol Exp Ther. 252: 643-50. PMID: 1968973
- Bile Acids Trigger GLP-1 Release Predominantly by Accessing Basolaterally Located G Protein-Coupled Bile Acid Receptors. | Brighton, CA., et al. 2015. Endocrinology. 156: 3961-70. PMID: 26280129
- An in silico approach to understand the structure-function properties of a serine protease (Bacifrinase) from Bacillus cereus and experimental evidence to support the interaction of Bacifrinase with fibrinogen and thrombin. | Bora, B., et al. 2017. J Biomol Struct Dyn. 35: 622-644. PMID: 26919276
- Angiotensin II Type 1 Receptor-Dependent GLP-1 and PYY Secretion in Mice and Humans. | Pais, R., et al. 2016. Endocrinology. 157: 3821-3831. PMID: 27447725
- Sirt1 Activity in PBMCs as a Biomarker of Different Heart Failure Phenotypes. | Conti, V., et al. 2020. Biomolecules. 10: PMID: 33238655
- Level of the SARS-CoV-2 receptor ACE2 activity is highly elevated in old-aged patients with aortic stenosis: implications for ACE2 as a biomarker for the severity of COVID-19. | Fagyas, M., et al. 2021. Geroscience. 43: 19-29. PMID: 33469835
- Nasal Delivery of Atenolol and Timolol in the Rat and the Effect of Absorption Enhancers. | Thadikonda, KP., et al. 1995. Drug Dev Ind Pharm. 21: 349-360. PMID: 36600544
- Inhibition of aminopeptidases by amastatin and bestatin derivatives. Effect of inhibitor structure on slow-binding processes. | Rich, DH., et al. 1984. J Med Chem. 27: 417-22. PMID: 6142952
- Amastatin, an inhibitor of aminopeptidase A, produced by actinomycetes. | Aoyagi, T., et al. 1978. J Antibiot (Tokyo). 31: 636-8. PMID: 681249
- X-ray crystallographic determination of the structure of bovine lens leucine aminopeptidase complexed with amastatin: formulation of a catalytic mechanism featuring a gem-diolate transition state. | Kim, H. and Lipscomb, WN. 1993. Biochemistry. 32: 8465-78. PMID: 8357796
Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
Amastatin hydrochloride, 1 mg | sc-202051 | 1 mg | $73.00 | |||
Amastatin hydrochloride, 5 mg | sc-202051A | 5 mg | $218.00 |
