MC 1293
Produktreferenzen ansehen (1)
Direktverknüpfungen
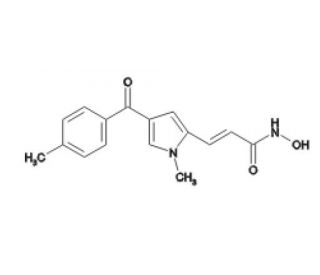
MC 1293 ist eine chemische Verbindung, die für ihre Rolle als Inhibitor der Histon-Deacetylase 1 (HDAC1) und der Mais-Histon-Deacetylase HD2 bekannt ist. Seine Hemmwirkung wird mit IC50-Werten von 4,5 µM für HDAC1 und 1,9 µM für HD2 aus Mais quantifiziert, was auf seine Wirksamkeit bei diesen spezifischen Konzentrationen hinweist. MC 1293 ist besonders wertvoll für die Untersuchung der Modulation der Chromatinstruktur durch epigenetische Mechanismen. HDAC-Inhibitoren wie MC 1293 werden eingesetzt, um zu erforschen, wie sich Veränderungen der Histonacetylierung auf die Organisation und Zugänglichkeit des Chromatins auswirken und dadurch die Zellfunktionen und die Genexpression beeinflussen. Dieser Forschungsbereich ist entscheidend für das Verständnis der grundlegenden Prozesse, die die zelluläre Regulierung und die Aufrechterhaltung der genomischen Integrität bestimmen. Da MC 1293 auf spezifische HDAC-Enzyme abzielt, dient es als nützliches experimentelles Werkzeug in der Molekularbiologie und Biochemie, um die Auswirkungen der Histon-Acetylierung auf verschiedene zelluläre Prozesse zu untersuchen. Die Spezifität und Wirksamkeit von MC 1293 bei der Hemmung bestimmter HDACs unterstreichen seine Bedeutung im Instrumentarium für die Erforschung der epigenetischen Regulierung.
MC 1293 Literaturhinweise
- 3-(4-Aroyl-1H-pyrrol-2-yl)-N-hydroxy-2-propenamide, eine neue Klasse synthetischer Histon-Deacetylase-Inhibitoren. | Massa, S., et al. 2001. J Med Chem. 44: 2069-72. PMID: 11405644
- Analyse des Bindungsmodus von 3-(4-Benzoyl-1-methyl-1H-2-pyrrolyl)-N-hydroxy-2-propenamid: ein neuer synthetischer Histon-Deacetylase-Inhibitor, der Histon-Hyperacetylierung, Wachstumshemmung und terminale Zelldifferenzierung bewirkt. | Mai, A., et al. 2002. J Med Chem. 45: 1778-84. PMID: 11960489
- Hemmung der iNOS-Expression und NO-Produktion durch entzündungshemmende Steroide. Umkehrung durch Histon-Deacetylase-Inhibitoren. | Hämäläinen, M., et al. 2008. Pulm Pharmacol Ther. 21: 331-9. PMID: 17913526
- Immunmodulatorische Wirkungen von Deacetylase-Inhibitoren: therapeutische Ausrichtung auf FOXP3+ regulatorische T-Zellen. | Wang, L., et al. 2009. Nat Rev Drug Discov. 8: 969-81. PMID: 19855427
- Histon-Deacetylase-Inhibitoren induzieren Apoptose bei menschlichen Eosinophilen und Neutrophilen. | Kankaanranta, H., et al. 2010. J Inflamm (Lond). 7: 9. PMID: 20181093
- Ein substratunabhängiger TR-FRET-Histon-Deacetylase-Inhibitor-Test. | Marks, BD., et al. 2011. J Biomol Screen. 16: 1247-53. PMID: 21940713
- Der Histon-Deacetylase-Inhibitor MC1293 induziert die Reaktivierung von latentem HIV-1 durch Histon-Modifikation in vitro-Latenz-Zelllinien. | Qu, X., et al. 2013. Curr HIV Res. 11: 24-9. PMID: 23092175
- Epigenetisch aufrechterhaltene SW13+ und SW13- Subtypen haben ein unterschiedliches onkogenes Potenzial und konvertieren mit HDAC1-Inhibition. | Davis, MR., et al. 2016. BMC Cancer. 16: 316. PMID: 27188282
- Die unterschiedlichen Rollen der RPD3-ähnlichen Histon-Deacetylasen der Klassen I und II bei der Reaktion auf Salinitätsstress. | Ueda, M., et al. 2017. Plant Physiol. 175: 1760-1773. PMID: 29018096
- Das LIM-Domänenprotein Ajuba ist ein notwendiger Kofaktor für den Gfi1-induzierten epigenetischen Schalter, der die Runx2-Unterdrückung in mit Multiplem Myelom exponierten Prä-Osteoblasten reguliert | Adamik, J., et al. 2015. Blood. 126(23): 4216.
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
MC 1293, 5 mg | sc-221875 | 5 mg | $202.00 |
