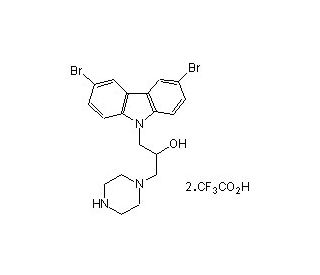
Bax channel blocker
Produktreferenzen ansehen (2)
Direktverknüpfungen
Bax Channel Blocker, ein zellpermeables Dibromocarbazolo-Piperazinyl-Derivat, weist starke anti-apoptotische Eigenschaften auf, die in erster Linie auf die Hemmung der Bax-Kanal-bildenden Aktivität zurückzuführen sind. Diese Verbindung ist in der Lage, die Freisetzung von Cytochrom c aus den Mitochondrien der HeLa-Zellen zu verhindern, ein Prozess, der normalerweise durch Bid, ein pro-apoptotisches Mitglied der Bcl-2-Familie, eingeleitet wird. Sein Wirkmechanismus besteht in der direkten Blockierung der Fähigkeit des Bax-Proteins, sich in die mitochondrialen Membranen zu integrieren und Kanäle zu bilden, ein wesentlicher Schritt auf dem intrinsischen Weg der Apoptose. Diese Wirkung unterstreicht nicht nur seinen potenziellen Nutzen bei der Entschlüsselung der molekularen Wege des Zelltods, sondern auch seine Bedeutung in Forschungsbereichen, die sich auf das Verständnis des komplizierten Gleichgewichts zwischen Zellüberleben und Apoptose konzentrieren. Durch die wirksame Modulation des Bax-vermittelten Apoptosewegs dient der Bax-Kanalblocker als wichtiges Instrument in der zell- und molekularbiologischen Forschung und bietet Einblicke in die Regulierung der Apoptose und ihre Auswirkungen auf die Aufrechterhaltung der zellulären Homöostase.
Bax channel blocker Literaturhinweise
- Azoxystrobin induziert die Apoptose menschlicher Plattenepithelkarzinome der Speiseröhre (KYSE-150) durch Auslösung des mitochondrialen Weges. | Shi, XK., et al. 2017. Front Pharmacol. 8: 277. PMID: 28567017
- Die Rückkopplungsaktivierung der AMPK-vermittelten Autophagie-Beschleunigung ist ein wichtiger Widerstandsmechanismus gegen die durch SCD1-Inhibitoren ausgelöste Hemmung des Zellwachstums. | Ono, A., et al. 2017. PLoS One. 12: e0181243. PMID: 28704514
- Einfluss von Bax und der mitochondrialen Permeabilitätsübergangspore auf die Cantharidin-induzierte Apoptose von Sf9-Zellen. | Cui, G., et al. 2017. Pestic Biochem Physiol. 142: 91-101. PMID: 29107253
- Die Aktivierung des apoptotischen Weges während der verlängerten Prometaphase blockiert die Proliferation der Tochterzellen. | Uetake, Y. and Sluder, G. 2018. Mol Biol Cell. 29: 2632-2643. PMID: 30133342
- Chemische Proteasom-Hemmung als neues Tiermodell für die innere Netzhautdegeneration bei Ratten. | Kageyama, M., et al. 2019. PLoS One. 14: e0217945. PMID: 31150519
- Optogenetische Störung der biochemischen Pfade, die das Zellverhalten steuern. | Haar, LL., et al. 2019. Methods Enzymol. 622: 309-328. PMID: 31155059
- Computergestützte Krebszellmodelle als Leitfaden für eine präzise Brustkrebsmedizin. | Cheng, L., et al. 2020. Genes (Basel). 11: PMID: 32121160
- Staurosporin und Venetoclax induzieren die Caspase-abhängige Proteolyse von MEF2D-Fusionsproteinen und Apoptose in MEF2D-Fusionszellen (+) der ALL. | Tange, N., et al. 2020. Biomed Pharmacother. 128: 110330. PMID: 32504922
- Aspirin induziert Gliom-Apoptose durch Noxa-Hochregulierung. | Chang, CY., et al. 2020. Int J Mol Sci. 21: PMID: 32545774
- Ipriflavon unterdrückt das Wachstum von Plattenepithelkarzinomen der Speiseröhre durch Hemmung von mTOR in vitro und in vivo. | Shi, X., et al. 2021. Front Oncol. 11: 648809. PMID: 34178634
- Antiapoptotischer Ansatz auf der Basis von pNiPAM-Nanopartikeln gegen die pro-regenerative Kapazität von myogenen Skelettzellen. | Nowaczyk, M., et al. 2021. Nanomaterials (Basel). 11: PMID: 34684935
- In-vitro-Studie der zytotoxischen Mechanismen von Alkylphospholipiden und Alkyltriazolen in Modellen der akuten lymphoblastischen Leukämie. | Jesus, LOP., et al. 2022. Molecules. 27: PMID: 36500726
- Chemische Aktivierung und mechanische Sensibilisierung von Piezo1 verstärken die TRAIL-vermittelte Apoptose in Glioblastomzellen. | Knoblauch, SV., et al. 2023. ACS Omega. 8: 16975-16986. PMID: 37214705
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
Bax channel blocker, 5 mg | sc-221285 | 5 mg | $152.00 |
