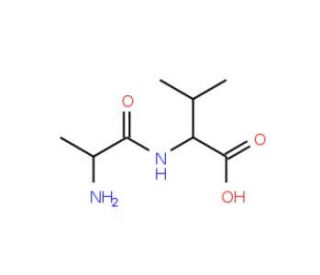
H-Ala-Val-OH (CAS 3303-45-5)
ACCÈS RAPIDE AUX LIENS
H-Ala-Val-OH est un composé dipeptidique qui sert d'élément constitutif dans la synthèse des peptides. Il joue un rôle dans la formation de chaînes peptidiques plus longues en fournissant une séquence spécifique d'acides aminés. Le H-Ala-Val-Oh interagit avec d'autres acides aminés et des liaisons peptidiques pour contribuer à l'assemblage de structures peptidiques complexes. Au niveau moléculaire, l'H-Ala-Val-OH participe à la formation des liaisons peptidiques grâce à sa structure chimique spécifique, permettant la liaison des acides aminés dans une séquence contrôlée. Le mécanisme d'action de l'H-Ala-Val-Oh implique sa réactivité chimique et sa capacité à former des liaisons covalentes avec d'autres acides aminés, facilitant ainsi la construction progressive des peptides. Le H-Ala-Val-OH sert de composant fondamental pour la synthèse de peptides avec des séquences spécifiques, contribuant ainsi à l'étude de la structure et de la fonction des peptides.
H-Ala-Val-OH (CAS 3303-45-5) Références
- Synthèse d'un nouveau dérivé de la duocarmycine DU-257 et son application à l'immunoconjugué utilisant un lien poly(éthylène glycol)-dipeptidyl capable d'activation spécifique de la tumeur. | Suzawa, T., et al. 2000. Bioorg Med Chem. 8: 2175-84. PMID: 11003162
- Synthèse et analyse HPLC d'un linker enzymatiquement clivable composé de poly(éthylène glycol) et d'un dipeptide pour le développement d'un immunoconjugué. | Suzawa, T., et al. 2000. J Control Release. 69: 27-41. PMID: 11018544
- Un système de nanotubes peptidiques exceptionnellement stable avec des pores flexibles. | Görbitz, CH. 2002. Acta Crystallogr B. 58: 849-54. PMID: 12324698
- Le collagène XXIV, un collagène fibrillaire vertébré présentant des caractéristiques structurelles des collagènes invertébrés: expression sélective dans la cornée et les os en développement. | Koch, M., et al. 2003. J Biol Chem. 278: 43236-44. PMID: 12874293
- Au-delà des nanotubes de carbone: les nanotubes de polypeptides comme alternatives ? | Praveena, G., et al. 2007. J Nanosci Nanotechnol. 7: 2253-9. PMID: 17663238
- Amélioration spectaculaire des signaux de pics croisés d'échange hyperpolarisés du xénon-129 en RMN 2D dans les nanotubes par interruption du flux de gaz. | Cheng, CY., et al. 2008. J Am Chem Soc. 130: 2390-1. PMID: 18237170
- Stockage du méthane, du dioxyde de carbone et de l'hydrogène dans des matériaux nanoporeux à base de dipeptides. | Comotti, A., et al. 2009. Chem Commun (Camb). 284-6. PMID: 19209303
- Effet des gènes de transporteurs d'efflux multidrogues sur la résistance et la surproduction de dipeptides chez Escherichia coli. | Hayashi, M., et al. 2010. FEMS Microbiol Lett. 304: 12-9. PMID: 20067529
- Interaction de la L-alanyl-L-valine et de la L-valyl-L-alanine avec des vapeurs organiques: stabilité thermique des clathrates, capacité de sorption et modification de la morphologie des films de dipeptides. | Ziganshin, MA., et al. 2015. Phys Chem Chem Phys. 17: 20168-77. PMID: 26179850
- Détermination précise et efficace de métabolites inconnus en métabolomique par l'identification de motifs moléculaires basée sur la RMN. | Wang, C., et al. 2019. Anal Chem. 91: 15686-15693. PMID: 31718151
- Auto-assemblage de peptides ultracourts: Les précurseurs du transport de médicaments et de gènes Cargos. | Gupta, S., et al. 2020. Front Bioeng Biotechnol. 8: 504. PMID: 32548101
- Conception d'un antidépresseur à action rapide en dissociant SERT de nNOS dans le DRN. | Sun, N., et al. 2022. Science. 378: 390-398. PMID: 36302033
- Site d'hydrolyse des dipeptides intestinaux. | Wiseman, G. 1977. J Physiol. 273: 731-43. PMID: 604456
- Sites d'hydrolyse des dipeptides en relation avec les sites de transport actif de l'histidine et du glucose dans l'intestin du hamster. | Wiseman, G. 1983. J Physiol. 342: 421-35. PMID: 6631743
- Absorption portale de petits peptides chez les rats dans des conditions de liberté. | Hara, H., et al. 1984. J Nutr. 114: 1122-9. PMID: 6726475
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
H-Ala-Val-OH, 1 g | sc-285876 | 1 g | $108.00 | |||
H-Ala-Val-OH, 5 g | sc-285876A | 5 g | $431.00 |
