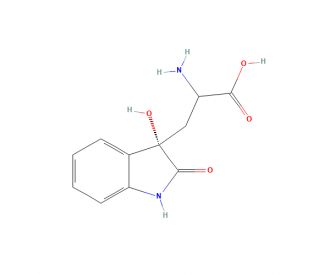
Dioxindolyl-L-alanine (CAS 184955-21-3)
ACCÈS RAPIDE AUX LIENS
La dioxindolyl-L-alanine joue un rôle dans le domaine de la synthèse peptidique, en particulier dans la création de peptides enrichis d'acides aminés uniques tels que le 5-Hydroxytryptophane, l'Oxindolylalanine, la N-Formylkynurénine et la Kynurénine. Son utilité découle de sa capacité à introduire ces acides aminés spécialisés dans des chaînes peptidiques, ce qui permet aux chercheurs d'explorer les voies et mécanismes biochimiques auxquels ces acides aminés participent. Plus précisément, l'inclusion de la Dioxindolyl-L-alanine dans la synthèse des peptides facilite l'étude du métabolisme du tryptophane et de ses effets en aval, qui sont essentiels à la compréhension de divers processus et réponses biologiques.
Dioxindolyl-L-alanine (CAS 184955-21-3) Références
- L'indole peut agir comme un signal extracellulaire pour réguler la formation du biofilm d'Escherichia coli et d'autres bactéries productrices d'indole. | Martino, PD., et al. 2003. Can J Microbiol. 49: 443-9. PMID: 14569285
- Mécanisme de liaison des analogues de substrat à la tryptophane indole-lyase: études utilisant la spectrophotométrie à balayage rapide et la spectrophotométrie à flux arrêté à longueur d'onde unique. | Phillips, RS., et al. 1990. Biochemistry. 29: 8608-14. PMID: 2271544
- Une preuve cinétique directe de la coexistence de 'l'adéquation induite' et de 'l'adéquation sélectionnée' dans le mécanisme de réaction d'une tryptophane indole lyase mutante Y72F de Proteus vulgaris. | Faleev, NG., et al. 2014. Biochim Biophys Acta. 1844: 1860-7. PMID: 25084024
- Structure cristalline de la tryptophane indole-lyase de Proteus vulgaris complexée avec l'oxindolyl-L-alanine: implications pour le mécanisme de réaction. | Phillips, RS., et al. 2018. Acta Crystallogr D Struct Biol. 74: 748-759. PMID: 30082510
- Détection et identification d'intermédiaires transitoires dans les réactions de la tryptophane synthase avec l'oxindolyl-L-alanine et le 2,3-dihydro-L-tryptophane. Preuve d'un intermédiaire tétraédrique (gem-diamine). | Roy, M., et al. 1988. Biochemistry. 27: 8661-9. PMID: 3064816
- Base structurale de la stéréochimie de l'inhibition de la tryptophane synthase par le tryptophane et ses dérivés. | Phillips, RS. and Harris, AP. 2021. Biochemistry. 60: 231-244. PMID: 33428374
- Inhibition différentielle de la tryptophane synthase et de la tryptophanase par les deux diastéréo-isomères du 2,3-dihydro-L-tryptophane. Implications pour la stéréochimie des intermédiaires réactionnels. | Phillips, RS., et al. 1985. J Biol Chem. 260: 14665-70. PMID: 3902836
- Interactions de la tryptophane synthase, de la tryptophanase et du phosphate de pyridoxal avec l'oxindolyl-L-alanine et le 2,3-dihydro-L-tryptophane: arguments en faveur d'un intermédiaire indolénique dans le métabolisme du tryptophane. | Phillips, RS., et al. 1984. Biochemistry. 23: 6228-34. PMID: 6395894
- Tryptophanase d'Escherichia coli: propriétés catalytiques et spectrales dans les solvants organiques de l'eau. | Faleev, NG., et al. 1994. Biochem Mol Biol Int. 34: 209-16. PMID: 7849621
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Dioxindolyl-L-alanine, 50 mg | sc-497015 | 50 mg | $434.00 |
