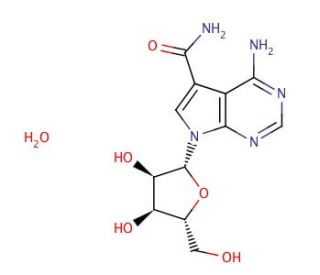
Structure moléculaire de Sangivamycin, Numéro CAS: 18417-89-5
Sangivamycin (CAS 18417-89-5)
Noms alternatifs:
7-Deaza-7-carbamoyladenosine
Application(s):
Sangivamycin est un nucléoside purique cytotoxique
Numéro CAS:
18417-89-5
Masse Moléculaire:
309.3
Formule Moléculaire:
C12H15N5O5
Information supplémentaire:
Ce produit est classé comme marchandise dangereuse pour le transport et peut faire l'objet de frais d'expédition supplémentaires.
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
La sangivamycine est un nucléoside purique cytotoxique actif contre le cytomégalovirus humain (HCMV). C'est également un inhibiteur sélectif et puissant de la PKC (protéine kinase C) (IC50 = 10muM). L'inhibition est compétitive par rapport à l'ATP et non compétitive par rapport aux cofacteurs histones et lipides. La phosphorylation de la protéine histone H1 est un mécanisme par lequel la sangivamycine empêche la croissance cellulaire et agit comme agent cytotoxique contre une variété de cancers humains.
Sangivamycin (CAS 18417-89-5) Références
- Synthèse de pyrrolo[2,1-f][1,2,4]triazine C-nucléosides. Isostères de sangivamycine, tubercidine et toyocamycine. | Nishimura, N., et al. 2001. Carbohydr Res. 331: 77-82. PMID: 11284507
- L'analogue nucléosidique sangivamycine induit une mort cellulaire apoptotique dans les cellules de carcinome mammaire MCF7/adriamycine résistantes via l'activation de la protéine kinase Cdelta et de JNK. | Lee, SA. and Jung, M. 2007. J Biol Chem. 282: 15271-83. PMID: 17371872
- Inhibition de l'angiogenèse tumorale en ciblant l'ATP synthase de la surface endothéliale avec la sangivamycine. | Komi, Y., et al. 2007. Jpn J Clin Oncol. 37: 867-73. PMID: 17956898
- L'ARC (NSC 188491) a une activité identique à celle de la sangivamycine (NSC 65346), y compris l'inhibition de la P-TEFb et de la PKC. | Stockwin, LH., et al. 2009. BMC Cancer. 9: 63. PMID: 19232100
- La sangivamycine induit l'apoptose en supprimant la signalisation Erk dans les cellules de lymphome à effusion primaire. | Wakao, K., et al. 2014. Biochem Biophys Res Commun. 444: 135-40. PMID: 24434142
- Comparaison des effets cellulaires et ARN-dépendants de la sangivamycine et de la toyocamycine sur des cellules humaines de carcinome du côlon. | Cohen, MB. and Glazer, RI. 1985. Mol Pharmacol. 27: 349-55. PMID: 2579317
- Synthèse, cytotoxicité et activité antivirale de certains analogues acycliques des antibiotiques nucléosides pyrrolo[2,3-d]pyrimidine tubercidine, toyocamycine et sangivamycine. | Gupta, PK., et al. 1989. J Med Chem. 32: 402-8. PMID: 2913300
- Un nouveau rôle biologique de la sangivamycine: l'inhibition des protéines kinases. | Osada, H., et al. 1989. J Antibiot (Tokyo). 42: 102-6. PMID: 2921215
- Pyrrolo[2,3-d]pyrimidine nucléosides comme inhibiteurs du cytomégalovirus humain. | Turk, SR., et al. 1987. Antimicrob Agents Chemother. 31: 544-50. PMID: 3037998
- La sangivamycine et ses dérivés inhibent la signalisation Haspin-Histone H3-survivin et induisent la mort des cellules cancéreuses du pancréas. | Bastea, LI., et al. 2019. Sci Rep. 9: 16588. PMID: 31719634
- La sangivamycine, un analogue nucléosidique, est un puissant inhibiteur de la protéine kinase C. | Loomis, CR. and Bell, RM. 1988. J Biol Chem. 263: 1682-92. PMID: 3338987
- La sangivamycine est très efficace contre le SRAS-CoV-2 in vitro et possède des propriétés médicamenteuses favorables. | Bennett, RP., et al. 2022. JCI Insight. 7: PMID: 34807849
- Composés liés aux acides nucléiques. 51. Synthèse et propriétés biologiques d'analogues modifiés par des sucres des antibiotiques nucléosides tubercidine, toyocamycine, sangivamycine et formycine. | De Clercq, E., et al. 1987. J Med Chem. 30: 481-6. PMID: 3820218
- Antibiotiques de type pyrrolo[2,3-d]pyrimidine nucléoside. Synthèse totale et structure de la toyocamycine, de l'unamycine B, du vengicide, de l'antibiotique E-212 et de la sangivamycine (BA-90912). | Tolman, RL., et al. 1968. J Am Chem Soc. 90: 524-6. PMID: 5634627
- Cinétique et localisation de la phosphorylation de la rhodopsine par la protéine kinase C. | Greene, NM., et al. 1995. J Biol Chem. 270: 6710-7. PMID: 7896814
Inhibiteur de:
ARPP-21, DERA, PKC, Ribosomal Protein L10a, Ser/Thr Protein Kinase, et U1 snRNP 70.Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Sangivamycin, 1 mg | sc-204261 | 1 mg | $333.00 | |||
Sangivamycin, 10 mg | sc-204261A | 10 mg | $1348.00 | |||
Sangivamycin, 25 mg | sc-204261B | 25 mg | $2611.00 | |||
Sangivamycin, 50 mg | sc-204261C | 50 mg | $5212.00 | |||
Sangivamycin, 100 mg | sc-204261D | 100 mg | $9894.00 | |||
Sangivamycin, 250 mg | sc-204261E | 250 mg | $20298.00 |
