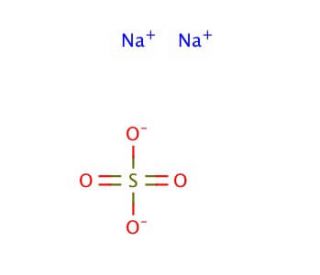
Sodium sulfate anhydrous (CAS 7757-82-6)
ACCÈS RAPIDE AUX LIENS
Le sulfate de sodium anhydre est un solide cristallin blanc. Le sulfate de sodium anhydre n'a pas de molécules d'eau dans sa structure, ce qui le distingue de la forme hydratée du sulfate de sodium. Ce composé chimique est largement utilisé dans les laboratoires et les industries en raison de ses propriétés polyvalentes. Il est utilisé comme agent de séchage, comme déshydratant et comme réactif dans les réactions chimiques. Le sulfate de sodium anhydre est soluble dans l'eau et a un point de fusion élevé, ce qui permet de l'utiliser dans des processus à haute température. D'un point de vue scientifique, le sulfate de sodium anhydre joue un rôle essentiel en chimie analytique. Il est utilisé dans l'analyse gravimétrique pour précipiter les ions baryum sous forme de sulfate de baryum, qui est insoluble dans l'eau. Cette propriété permet de déterminer les concentrations d'ions sulfate dans divers échantillons. En outre, il est utilisé dans la synthèse d'autres composés chimiques et dans la recherche impliquant la cristallographie et les sciences des matériaux. Le mécanisme d'action du sulfate de sodium anhydre est principalement attribué à sa capacité à agir comme un agent déshydratant. Il absorbe facilement l'eau de son environnement, ce qui le rend efficace pour éliminer l'humidité ou la teneur en eau des substances. Cette propriété permet de maintenir la pureté et la stabilité de certains composés chimiques, ainsi que de faciliter la conservation de divers matériaux. Le sulfate de sodium anhydre est présent dans les environnements arides sous forme de thénardite minérale, mais le décahydrate (sc-203405) est la forme naturelle la plus abondante et est dérivé du minéral mirabilite, que l'on trouve souvent dans les fonds lacustres.
Sodium sulfate anhydrous (CAS 7757-82-6) Références
- [Capacité de séchage du sulfate de sodium anhydre sur les solvants organiques humides après partition liquide-liquide]. | Obana, H., et al. 2001. Shokuhin Eiseigaku Zasshi. 42: 148-53. PMID: 11486383
- Analyse du furanéol dans les tomates par échantillonnage dynamique de l'espace de tête avec du sulfate de sodium. | Buttery, RG., et al. 2001. J Agric Food Chem. 49: 4349-51. PMID: 11559136
- Études sur la proportion relative des fractions d'albumine et de globuline sériques déterminées par précipitation au méthanol et au sulfate de sodium. | ALHA, AL. 1949. Ann Chir Gynaecol Fenn Suppl. 38: 6-17. PMID: 15394523
- Caractérisation in situ d'hydrates de sel insaisissables. Structures cristallines de l'heptahydrate et de l'octahydrate de sulfate de sodium. | Oswald, ID., et al. 2008. J Am Chem Soc. 130: 17795-800. PMID: 19053442
- Facteurs affectant la taille et le gonflement des microsphères de poly(éthylène glycol) formées dans des solutions aqueuses de sulfate de sodium sans tensioactifs. | Nichols, MD., et al. 2009. Biomaterials. 30: 5283-91. PMID: 19615738
- Fractionnement des protéines sériques: comparaison entre la précipitation au sulfate de sodium et l'électrophorèse. | MILNE, J. 1947. J Biol Chem. 169: 595-9. PMID: 20259092
- Dommages dans les milieux poreux dus à la cristallisation du sel. | Shahidzadeh-Bonn, N., et al. 2010. Phys Rev E Stat Nonlin Soft Matter Phys. 81: 066110. PMID: 20866481
- [Détermination du butroxydime dans les produits agricoles par LC-MS]. | Minatani, T., et al. 2015. Shokuhin Eiseigaku Zasshi. 56: 233-9. PMID: 26699270
- Détermination du photo-initiateur 4-méthylbenzophénone dans le lait par extraction du point de trouble. | Ding, S., et al. 2016. J Sep Sci. 39: 4027-4034. PMID: 27569853
- L'importance de la préparation de l'intestin à la coloscopie pour la détection des lésions colorectales et la prévention du cancer colorectal. | Sharma, P., et al. 2020. Endosc Int Open. 8: E673-E683. PMID: 32355887
- Détermination de multiples antibiotiques dans les sols agricoles à l'aide d'une méthode rapide, facile, bon marché, efficace, robuste et sûre couplée à la chromatographie liquide à ultra-haute performance et à la spectrométrie de masse en tandem. | Zhang, Y., et al. 2022. J Sep Sci. 45: 602-613. PMID: 34750965
- Détermination de huit insecticides néonicotinoïdes dans le chou chinois à l'aide d'une méthode QuEChERS modifiée combinée à la chromatographie liquide ultra performante et à la spectrométrie de masse en tandem. | Yang, B., et al. 2022. Food Chem. 387: 132935. PMID: 35427864
- Un support de type cellulose pour le couplage intime de la photocatalyse et de la biodégradation. | Wan, Z., et al. 2022. Polymers (Basel). 14: PMID: 35893962
- Détermination rapide de 103 résidus de médicaments vétérinaires courants dans le lait et les produits laitiers par chromatographie liquide ultra performante et spectrométrie de masse en tandem. | Guo, X., et al. 2022. Front Nutr. 9: 879518. PMID: 35938118
- Première étude de principe sur la stabilité des passivations de Cd dans le sol. | Shen, J., et al. 2023. Sci Rep. 13: 4255. PMID: 36918623
- Absorption du sulfate de sodium administré par voie orale chez l'homme. | Cocchetto, DM. and Levy, G. 1981. J Pharm Sci. 70: 331-3. PMID: 7264905
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Sodium sulfate anhydrous, 500 g | sc-212945 | 500 g | $63.00 | |||
Sodium sulfate anhydrous, 1 kg | sc-212945A | 1 kg | $91.00 |
