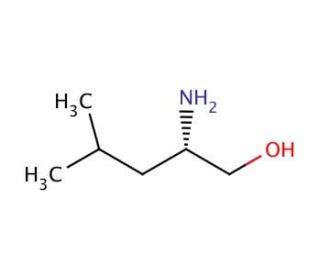
(S)-(+)-Leucinol (CAS 7533-40-6)
ACCÈS RAPIDE AUX LIENS
Le (S)-(+)-Leucinol est un composé qui fonctionne comme un élément de construction chiral dans la synthèse organique. Il sert d'intermédiaire clé dans la production de divers produits agrochimiques et de produits chimiques fins. Le mécanisme d'action du composé consiste à participer à la synthèse asymétrique, où il agit comme auxiliaire ou ligand chiral dans les réactions catalytiques. Cela permet de créer des composés énantiomériquement purs, ce qui est utile pour le développement de nouvelles entités chimiques et de nouveaux matériaux. Le rôle fonctionnel du (S)-(+)-leucinol réside dans sa capacité à faciliter la formation de liaisons stéréosélectives, ce qui permet la synthèse de molécules complexes avec des niveaux élevés de contrôle stéréochimique. Le (S)-(+)-Leucinol joue un rôle important dans l'avancement des méthodologies et la préparation de composés optiquement purs à diverses fins de recherche et de développement.
(S)-(+)-Leucinol (CAS 7533-40-6) Références
- La signalisation eIF2α hypothalamique régule la prise alimentaire. | Maurin, AC., et al. 2014. Cell Rep. 6: 438-44. PMID: 24485657
- Réaction d'aldol croisé de l'isatine avec l'acétone catalysée par le leucinol: Une étude mécaniste. | Kabeshov, MA., et al. 2015. Chemistry. 21: 12026-33. PMID: 26147182
- Rhizoleucinoside, un hybride rhamnolipide-alcool aminé provenant du symbiote rhizobien Bradyrhizobium sp. BTAi1. | Chen, J., et al. 2016. Org Lett. 18: 1490-3. PMID: 26959412
- Synthèse totale des fellutamides, inhibiteurs lipopeptidiques du protéasome. Formation de liaisons peptidiques plus durables. | Pirrung, MC., et al. 2016. Org Biomol Chem. 14: 8367-75. PMID: 27533920
- Synthèse multicomposante en une étape de complexes oxazolinyl-zinc chiraux. | Luo, M., et al. 2017. Chem Cent J. 11: 81. PMID: 29086857
- La fusaoctaxine A, un exemple de mécanisme en deux étapes pour l'assemblage et la maturation des peptides non ribosomaux chez les champignons. | Westphal, KR., et al. 2019. Toxins (Basel). 11: PMID: 31100892
- Une nouvelle classe de dérivés α-cétoamides avec de puissantes activités anticancéreuses et anti-SARS-CoV-2. | Wang, J., et al. 2021. Eur J Med Chem. 215: 113267. PMID: 33639344
- Désaturation radicale à distance des liaisons C-H non activées dans les amides. | Xia, Y., et al. 2021. Chemistry. 27: 16621-16625. PMID: 34590351
- Nystatine hydrosoluble et dérivés. | Amir, A., et al. 2022. ACS Med Chem Lett. 13: 182-187. PMID: 35178173
- Une série de bis-aminotriazines substituées sont des activateurs du récepteur C du peptide natriurétique. | Smith, RJ., et al. 2022. J Med Chem. 65: 5495-5513. PMID: 35333039
- Le cloisonnement des étapes catalytiques initiales de la leucyl-ARNt synthétase est piloté par un retournement peptide-plan du site actif. | Pang, L., et al. 2022. Commun Biol. 5: 883. PMID: 36038645
- Synthèse stéréosélective d'oxindoles C3-tétrasubstitués par propargylation asymétrique catalysée par le cuivre. | Wang, JM., et al. 2022. RSC Adv. 12: 26727-26732. PMID: 36320842
- Synthèse facile de 2-Oxazolines par cyclisation déshydrative favorisée par l'acide triflique. | Yang, T., et al. 2022. Molecules. 27: PMID: 36558175
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
(S)-(+)-Leucinol, 5 g | sc-258127 | 5 g | $68.00 | |||
(S)-(+)-Leucinol, 25 g | sc-258127A | 25 g | $332.00 |
