OU749 (CAS 519170-13-9)
QUICK LINKS
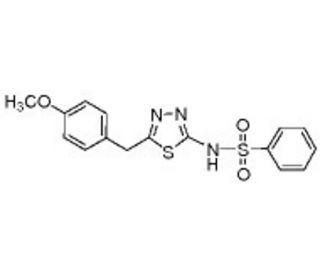
OU749, known as N-[5-[(4-Methoxyphenyl)methyl]-1,3,4-thiadiazol-2-yl]-benzenesulfonamide, is notable in research for its role as a non-glutamine uncompetitive inhibitor of gamma-glutamyl transpeptidase (GGT), an enzyme involved in glutathione metabolism and amino acid transport. By inhibiting GGT, OU749 is used to study the enzyme′s function in these critical biological processes, and its uncompetitive inhibition suggests that it binds to the enzyme-substrate complex, offering a unique angle to explore GGT′s enzymatic kinetics and potential regulatory mechanisms. The compound′s thiadiazole and benzenesulfonamide moieties may contribute to its binding affinity and specificity, making it a valuable probe for elucidating the structural requirements for GGT inhibition. Researchers utilize OU749 to dissect the enzyme′s role in cellular processes, such as oxidative stress response and detoxification pathways, which can lead to a deeper understanding of GGT′s involvement in biological systems and contribute to the design of novel inhibitors with potential research applications.
OU749 (CAS 519170-13-9) References
- A novel, species-specific class of uncompetitive inhibitors of gamma-glutamyl transpeptidase. | King, JB., et al. 2009. J Biol Chem. 284: 9059-65. PMID: 19203993
- Divergent effects of compounds on the hydrolysis and transpeptidation reactions of γ-glutamyl transpeptidase. | Wickham, S., et al. 2012. J Enzyme Inhib Med Chem. 27: 476-89. PMID: 21864033
- Probing the donor and acceptor substrate specificity of the γ-glutamyl transpeptidase. | Hu, X., et al. 2012. Biochemistry. 51: 1199-212. PMID: 22257032
- Inhibition of human γ-glutamyl transpeptidase: development of more potent, physiologically relevant, uncompetitive inhibitors. | Wickham, S., et al. 2013. Biochem J. 450: 547-57. PMID: 23301618
- Controversial role of gamma-glutamyl transferase activity in cisplatin nephrotoxicity. | Fliedl, L., et al. 2014. ALTEX. 31: 269-78. PMID: 24664430
- Human γ-Glutamyl Transpeptidase 1: STRUCTURES OF THE FREE ENZYME, INHIBITOR-BOUND TETRAHEDRAL TRANSITION STATES, AND GLUTAMATE-BOUND ENZYME REVEAL NOVEL MOVEMENT WITHIN THE ACTIVE SITE DURING CATALYSIS. | Terzyan, SS., et al. 2015. J Biol Chem. 290: 17576-86. PMID: 26013825
- Crosstalk between cystine and glutathione is critical for the regulation of amino acid signaling pathways and ferroptosis. | Yu, X. and Long, YC. 2016. Sci Rep. 6: 30033. PMID: 27425006
- Gamma-Glutamyltransferase 1 Promotes Clear Cell Renal Cell Carcinoma Initiation and Progression. | Bansal, A., et al. 2019. Mol Cancer Res. 17: 1881-1892. PMID: 31151999
- Arsenic induced alteration in Mrp-1 like activity leads to zebrafish hepatocyte apoptosis: The cellular GSH connection. | Ray, A., et al. 2020. Environ Toxicol Pharmacol. 79: 103427. PMID: 32470611
- A Systematic Review of Serum γ-Glutamyltransferase as a Prognostic Biomarker in Patients with Genitourinary Cancer. | Takemura, K., et al. 2021. Antioxidants (Basel). 10: PMID: 33916150
- Fighting against drug-resistant tumors by the inhibition of γ-glutamyl transferase with supramolecular platinum prodrug nano-assemblies. | Wang, L., et al. 2021. J Mater Chem B. 9: 4587-4595. PMID: 34059856
- Expression of gamma-glutamyltransferase 1 in glioblastoma cells confers resistance to cystine deprivation-induced ferroptosis. | Hayashima, K. and Katoh, H. 2022. J Biol Chem. 298: 101703. PMID: 35148992
- Design and evaluation of novel analogs of 2-amino-4-boronobutanoic acid (ABBA) as inhibitors of human gamma-glutamyl transpeptidase. | Nguyen, L., et al. 2022. Bioorg Med Chem. 73: 116986. PMID: 36208545
Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
OU749, 5 mg | sc-253219 | 5 mg | $132.00 |
