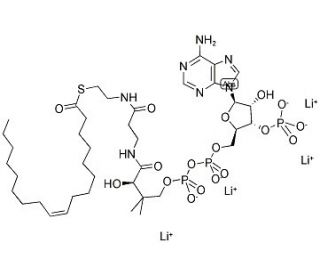
Oleoyl coenzyme A lithium salt (CAS 188824-37-5)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
Le sel de lithium de l'oléoyl coenzyme A est un intermédiaire dans le processus de métabolisation des acides gras au sein des cellules. Il joue un rôle clé dans le transport des acides gras à longue chaîne vers les mitochondries, où ils subissent une bêta-oxydation pour produire de l'énergie. Le sel de lithium de l'oléoyl coenzyme A interagit avec diverses enzymes et protéines porteuses impliquées dans le métabolisme des acides gras, facilitant le transfert des acides gras à travers les membranes cellulaires et dans les mitochondries. Ce faisant, il contribue à la régulation de la production d'énergie cellulaire et de l'homéostasie lipidique. Le sel de lithium de l'oléoyl coenzyme A participe à la synthèse de lipides complexes, tels que les phospholipides et les triglycérides, qui sont des composants clés des membranes cellulaires et du stockage de l'énergie. Sa présence est essentielle au bon fonctionnement des processus cellulaires et des voies liées au métabolisme énergétique et à la synthèse des lipides.
Oleoyl coenzyme A lithium salt (CAS 188824-37-5) Références
- Acylation de la monolysocardiolipine dans le cœur de rat. | Ma, BJ., et al. 1999. J Lipid Res. 40: 1837-45. PMID: 10508203
- La synthèse des acides gras dans les plastes des racines de pois est inhibée par l'action des acyl-coenzymes à longue chaîne sur les transporteurs de métabolites. | Fox, SR., et al. 2001. Plant Physiol. 126: 1259-65. PMID: 11457976
- Comparaison du métabolisme de l'acide oléique dans le soja (Glycine max [L.] Merr.), génotypes Williams et A5, un mutant présentant une diminution de l'acide linoléique dans la graine. | Martin, BA. and Rinne, RW. 1986. Plant Physiol. 81: 41-4. PMID: 16664804
- La synthèse des esters de cire est nécessaire pour que Mycobacterium tuberculosis entre en dormance in vitro. | Sirakova, TD., et al. 2012. PLoS One. 7: e51641. PMID: 23272127
- L'oleoyl coenzyme A régule l'interaction du régulateur transcriptionnel RaaS (Rv1219c) avec l'ADN chez les mycobactéries. | Turapov, O., et al. 2014. J Biol Chem. 289: 25241-9. PMID: 25012658
- L'agrégation plaquettaire est inhibée par l'acyl-CoA à longue chaîne. | Lascu, I., et al. 1988. Biochem Biophys Res Commun. 156: 1020-5. PMID: 3142460
- Rôle de l'acyl-coenzyme A oxydase dans l'efflux de glutathion oxydé à partir de foies perfusés de rats traités avec la nafenopine, un proliférateur de peroxysomes. | Conway, JG., et al. 1987. Cancer Res. 47: 4795-800. PMID: 3621175
- Transport d'adénine nucléotide sensible à l'acyl-coenzyme A dans un système de liposomes reconstitués. | Woldegiorgis, G., et al. 1981. J Biol Chem. 256: 12297-300. PMID: 6271781
- Nouvelle formation de S-méthylacylthioester à partir de l'oléoyl-coenzyme A et de la S-adénosylméthionine en présence de FeSO4. | Zatz, M., et al. 1983. J Biol Chem. 258: 5759-63. PMID: 6853544
- Interaction de l'oleoyl coenzyme A avec les bicouches phospholipidiques. | Lichtenstein, AH., et al. 1982. Biochemistry. 21: 2233-41. PMID: 7093242
- Biosynthèse du S-méthyl-N-oléoylmercaptoéthylamide à partir de l'oléoyl-coenzyme A et de la S-adénosylméthionine. | Zatz, M., et al. 1982. J Biol Chem. 257: 13673-8. PMID: 7142172
- Analyse de la liaison de l'acyl-coenzyme A au facteur de transcription FadR et identification des résidus d'acides aminés dans l'extrémité carboxyle nécessaires à la liaison du ligand. | Raman, N. and DiRusso, CC. 1995. J Biol Chem. 270: 1092-7. PMID: 7836365
- L'acylation du lysophosphatidylglycérol dans le cœur de rat: preuves d'activités in vitro et in vivo. | Cheng, P., et al. 1996. Biochim Biophys Acta. 1302: 61-8. PMID: 8695656
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Oleoyl coenzyme A lithium salt, 5 mg | sc-215626 | 5 mg | $216.00 | |||
Oleoyl coenzyme A lithium salt, 10 mg | sc-215626A | 10 mg | $379.00 |
