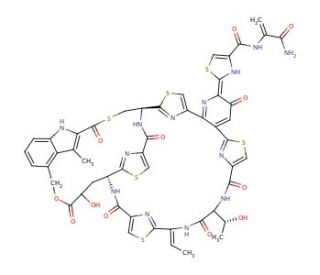
Nosiheptide (CAS 56377-79-8)
ACCÈS RAPIDE AUX LIENS
Le nosiheptide, également connu sous le nom de multhiomycine, est un thiopeptide produit par la bactérie Streptomyces actuosus. Il a été largement étudié pour sa capacité à cibler la sous-unité 50S des ribosomes bactériens, en se liant spécifiquement à l'ARNr 23S près du centre de la peptidyltransférase. Cette interaction perturbe effectivement la fonction ribosomale en inhibant la formation de liaisons peptidiques entre les acides aminés au cours de la synthèse des protéines. Ce mécanisme a fait du nosiheptide un outil essentiel pour les chercheurs qui étudient la synthèse des protéines bactériennes et la structure des ribosomes. Il constitue une sonde moléculaire permettant d'élucider les subtilités de l'inhibition de la traduction et de la dynamique des ribosomes. Les études structurelles, qui font appel à des techniques avancées telles que la cristallographie aux rayons X et la cryo-microscopie électronique, ont bénéficié de l'utilisation du nosiheptide pour mieux comprendre les interactions et la stabilité des ribosomes. En outre, l'impact de la nosiheptide s'étend au domaine de l'ingénierie des ribosomes et de la biologie synthétique. Les connaissances acquises grâce à son interaction avec le ribosome sont exploitées pour concevoir des ribosomes modifiés dotés de nouvelles capacités, améliorant ainsi les applications biotechnologiques.
Nosiheptide (CAS 56377-79-8) Références
- Organisation transcriptionnelle et régulation du gène de résistance au nosiheptide chez Streptomyces actuosus. | Li, Y., et al. 1991. J Ind Microbiol. 8: 1-12. PMID: 1367329
- Opportunités et défis des recherches actuelles sur la logique de biosynthèse des antibiotiques thiopeptides représentés par le nosiheptide. | Wang, S., et al. 2013. Curr Opin Chem Biol. 17: 626-34. PMID: 23838388
- L'importance du codon de départ de nosM dans la production de nosiheptide. | Jiang, L., et al. 2015. Chin J Nat Med. 13: 854-860. PMID: 26614460
- Amélioration de la production de nosiheptide chez Streptomyces actuosus par l'expression hétérologue de l'hémoprotéine de Sinorhizobium meliloti. | Mo, Q., et al. 2016. Lett Appl Microbiol. 62: 480-7. PMID: 27096926
- Synthèse totale du Nosiheptide. | Wojtas, KP., et al. 2016. Angew Chem Int Ed Engl. 55: 9772-6. PMID: 27345011
- La mutagenèse du peptide leader de NosM révèle des éléments importants dans la biosynthèse du Nosiheptide. | Jin, L., et al. 2017. Appl Environ Microbiol. 83: PMID: 27913416
- Analogues du nosiheptide comme agents antibactériens potentiels via des modifications de la région de la déhydroalanine: Semi-synthèse, activité antimicrobienne et étude d'ancrage moléculaire. | Fan, Y., et al. 2021. Bioorg Med Chem. 31: 115970. PMID: 33422909
- Détermination directe des résidus de nosiheptide dans les tissus animaux par chromatographie liquide et spectrométrie de masse en tandem. | Shen, J., et al. 2022. J Chromatogr B Analyt Technol Biomed Life Sci. 1193: 123167. PMID: 35196626
- La mutasynthèse génère des analogues antibactériens du nosiheptide contenant du benzothiophène. | Mu, N., et al. 2022. J Nat Prod. 85: 2274-2281. PMID: 36122372
- Le nosiheptide possède de puissantes activités inhibitrices in vitro et intracellulaires contre Mycobacterium tuberculosis. | Yu, X., et al. 2022. Microbiol Spectr. 10: e0144422. PMID: 36222690
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Nosiheptide, 1 mg | sc-397320 | 1 mg | $290.00 |
