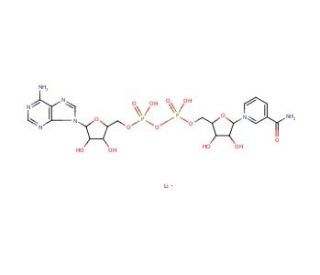
NAD+, Lithium Salt (CAS 64417-72-7)
ACCÈS RAPIDE AUX LIENS
Le NAD+, sel de lithium est une variante du nicotinamide adénine dinucléotide où les ions lithium sont utilisés pour neutraliser la charge négative de la molécule de NAD+. En recherche, cette forme de sel est particulièrement utile dans les réactions enzymatiques et les études impliquant les déshydrogénases, où il agit comme un coenzyme essentiel aux réactions d'oxydoréduction. Le sel de lithium NAD+ est utilisé pour étudier les voies métaboliques et la production d'énergie, car il participe à la chaîne de transport d'électrons dans les mitochondries cellulaires. Il joue également un rôle important dans les études sur la réparation de l'ADN, étant donné son rôle de substrat pour les ADP-ribosyltransférases. En outre, les chercheurs utilisent le NAD+, sel de lithium dans des essais visant à mesurer l'activité des sirtuines et des PARP, qui sont importants pour comprendre la régulation cellulaire, les réponses au stress et le maintien de la stabilité génomique.
NAD+, Lithium Salt (CAS 64417-72-7) Références
- Régulation enzymatique par inhibition réversible du zinc: exemple de la glycérol phosphate déshydrogénase. | Maret, W., et al. 2001. Chem Biol Interact. 130-132: 891-901. PMID: 11306104
- Procédures de référence primaires de l'IFCC pour la mesure des concentrations d'activité catalytique des enzymes à 37 degrés C. Partie 3. Procédure de référence pour la mesure de la concentration catalytique de la lactate déshydrogénase. | Schumann, G., et al. 2002. Clin Chem Lab Med. 40: 643-8. PMID: 12211663
- Dosage du l- et du d-Lactate dans des échantillons de lait réel avec des réacteurs enzymatiques immobilisés et une électrode en graphite. | Marrazza, G., et al. 1994. Talanta. 41: 1007-14. PMID: 18966029
- Procédures de référence de l'IFCC pour la mesure des concentrations catalytiques des enzymes: corrigendum, notes et conseils utiles. Fédération internationale de chimie clinique et de médecine de laboratoire (IFCC) -- Division scientifique de l'IFCC. | Schumann, G., et al. 2010. Clin Chem Lab Med. 48: 615-21. PMID: 20298135
- Détermination de l'activité de la lactate déshydrogénase dans les tumeurs par la mesure de l'échange hydrogène/deutérium dans le l-[1-(13)C,U-(2)H]lactate hyperpolarisé. | Kennedy, BW., et al. 2012. J Am Chem Soc. 134: 4969-77. PMID: 22316419
- Inversion d'une partie de la voie réactionnelle de l'aldéhyde déshydrogénase lors de l'hydrolyse d'un ester. | Duncan, RJ. 1979. Biochem J. 183: 459-62. PMID: 230823
- Transporteurs d'oxygène à base d'hémoglobine PEGylée à haute et faible affinité: Stress oxydatif différentiel dans un modèle de transfusion chez le cochon d'Inde. | Alomari, E., et al. 2018. Free Radic Biol Med. 124: 299-310. PMID: 29920341
- Structure de l'adénosine-5'-mononicotinate (AMN) trihydraté: un analogue du NAD pour tester l'empilement intramoléculaire. | Ramasubbu, N. and Parthasarathy, R. 1988. Acta Crystallogr C. 44 (Pt 12): 2140-4. PMID: 3270554
- La simvastatine altère l'homéostasie du glucose chez la souris en fonction de l'expression du muscle squelettique PGC-1α. | Panajatovic, MV., et al. 2020. Biomedicines. 8: PMID: 32942550
- Modification de la lactate déshydrogénase testiculaire de souris par le pyridoxal 5'-phosphate. | Gould, KG. and Engel, PC. 1980. Biochem J. 191: 365-71. PMID: 6786279
- La pyruvate décarboxylase catalyse la décarboxylation des acides 2-oxo à chaîne ramifiée mais n'est pas essentielle à la production d'alcool de fusel par Saccharomyces cerevisiae. | ter Schure, EG., et al. 1998. Appl Environ Microbiol. 64: 1303-7. PMID: 9546164
- Méthode enzymatique pour l'oxalate automatisée à l'aide de l'analyseur Hitachi 911. | Langman, LJ. and Allen, LC. 1998. Clin Biochem. 31: 429-32. PMID: 9721445
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
NAD+, Lithium Salt, 1 g | sc-208085 | 1 g | $272.00 |
