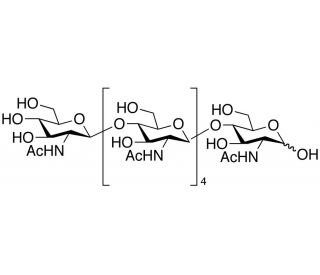
N,N′,N″,N‴,N⁗,N⁗′-Hexaacetylchitohexaose (CAS 38854-46-5)
Voir les citations produits (3)
ACCÈS RAPIDE AUX LIENS
N,N',N'',N''',N'''',N'''''-Hexaacetylchitohexaose est un oligosaccharide chimiquement modifié qui est largement utilisé dans la recherche biochimique pour étudier les interactions glucides-protéines, en particulier celles impliquant la chitine et ses dérivés. En tant qu'analogue soluble de la chitine, il constitue un modèle précieux pour comprendre la spécificité de liaison et les processus enzymatiques liés à ce polymère naturel. Les chercheurs utilisent cet hexamère pour étudier la spécificité du substrat des chitinases, enzymes responsables de la dégradation de la chitine, ce qui est important pour explorer le cycle de vie des organismes contenant de la chitine et le développement d'agents de biocontrôle. Les groupes Acétyle du composé améliorent sa solubilité, ce qui le rend particulièrement utile dans les essais in vitro pour imiter la structure de la chitine sous une forme plus accessible. En outre, il est utilisé dans le domaine de la glycobiologie pour étudier la structure et la fonction des liaisons glycosidiques et pour explorer les mécanismes de la glycosylation, un processus vital pour le bon fonctionnement des cellules.
N,N′,N″,N‴,N⁗,N⁗′-Hexaacetylchitohexaose (CAS 38854-46-5) Références
- Études de RMN et de modélisation des interactions protéine-glucide: synthèse, structure tridimensionnelle et propriétés de reconnaissance d'un domaine d'hévéine minimum ayant une affinité de liaison pour les chitooligosaccharides. | Aboitiz, N., et al. 2004. Chembiochem. 5: 1245-55. PMID: 15368576
- Domaines d'hévéine: un modèle attrayant pour étudier les interactions glucides-protéines à une résolution atomique. | Jiménez-Barbero, J., et al. 2006. Adv Carbohydr Chem Biochem. 60: 303-54. PMID: 16750446
- Mesure des interactions protéine-ligand à l'aide de la spectrométrie de masse par désorption d'échantillons liquides et ionisation par électronébulisation. | Liu, P., et al. 2013. Anal Chem. 85: 11966-72. PMID: 24237005
- Électrochimie des protéines et glycoprotéines non conjuguées. Vers des capteurs pour la biomédecine et la glycomique. | Paleček, E., et al. 2015. Chem Rev. 115: 2045-108. PMID: 25659975
- Aperçu structurel de la reconnaissance de la paroi cellulaire fongique par une protéine CVNH dotée d'un seul domaine LysM. | Koharudin, LM., et al. 2015. Structure. 23: 2143-54. PMID: 26455798
- Une chitinase structurellement nouvelle provenant de l'archéon hyperthermophile dégradant la chitine Thermococcus chitonophagus. | Horiuchi, A., et al. 2016. Appl Environ Microbiol. 82: 3554-3562. PMID: 27060120
- Structures cristallines d'une chitinase archéenne ChiD et de ses complexes de ligands. | Nishitani, Y., et al. 2018. Glycobiology. 28: 418-426. PMID: 29800365
- Rôle des résidus lysine de l'effecteur AvrPiz-t de Magnaporthe oryzae dans l'immunité déclenchée par l'effecteur et le PAMP. | Bai, P., et al. 2019. Mol Plant Pathol. 20: 599-608. PMID: 30548752
- Voltampérométrie cyclique et à ondes carrées de chitooligosaccharides modifiés par l'osmium(VI) tétraméthyléthylènediamine. | Trefulka, M. and Ostatná, V. 2020. Bioelectrochemistry. 133: 107494. PMID: 32120319
- Structure à résolution 1,8 A de l'hevamine, une chitinase/lysozyme végétale, et analyse de la séquence conservée et des motifs de structure de la famille 18 des glycosyl hydrolases. | Terwisscha van Scheltinga, AC., et al. 1996. J Mol Biol. 262: 243-57. PMID: 8831791
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
N,N′,N″,N‴,N⁗,N⁗′-Hexaacetylchitohexaose, 1 mg | sc-222018 | 1 mg | $228.00 | |||
N,N′,N″,N‴,N⁗,N⁗′-Hexaacetylchitohexaose, 5 mg | sc-222018A | 5 mg | $416.00 | |||
N,N′,N″,N‴,N⁗,N⁗′-Hexaacetylchitohexaose, 25 mg | sc-222018B | 25 mg | $1883.00 |
