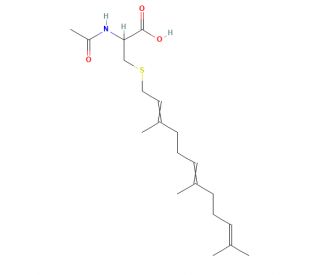
N-Acetyl-S-farnesyl-L-cysteine (AFC) (CAS 135304-07-3)
ACCÈS RAPIDE AUX LIENS
La N-Acétyle-S-farnésyl-L-cystéine (AFC) est un acide aminé cystéine dérivé synthétiquement qui inhibe les enzymes S-farnésylcystéine carboxyl méthyltransférase. Ces enzymes reconnaissent la N-acétyl-S-farnésyl-L-cystéine (AFC) comme substrat par l'intermédiaire du groupement farnésyl, et l'occupation du site de liaison bloque la transformation des protéines farnésylées par l'enzyme. La méthylation carboxyle des protéines farnésylées est une modification importante qui régule la fonction des protéines. Le blocage du traitement par la méthyltransférase des protéines rap1 plaquettaires par la N-Acétyle-S-farnésyl-L-cystéine (AFC) conduit à l'inhibition de l'agrégation plaquettaire. La N-acétyl-S-farnésyl-L-cystéine (AFC) est également décrite pour bloquer le mouvement cellulaire et l'adhésion membranaire des protéines Ras en interférant avec le traitement de méthylation carboxyle. L'Acétyle-S-farnésyl-L-cystéine (AFC) en tant que substrat de la méthyltransférase des protéines isoprénylées est décrit pour bloquer la libération de l'anion radical superoxyde stimulée par le fMet-Leu-Phe dans les cellules neutrophiles. L'inhibition de la chimiotaxie des neutrophiles par la N-acétyle-S-farnésyl-L-cystéine (AFC) entraîne également la suppression de la réponse inflammatoire induite par le 12-O-tereadecanoyl-phorbol-13-acetate et l'acide arachidonique.
N-Acetyl-S-farnesyl-L-cysteine (AFC) (CAS 135304-07-3) Références
- La méthylation carboxyle de Ras régule le ciblage de la membrane et l'engagement de l'effecteur. | Chiu, VK., et al. 2004. J Biol Chem. 279: 7346-52. PMID: 14660603
- Stimulation de l'activité de Rac1 par le facteur de nécrose tumorale alpha. Rôle de l'isoprénylcystéine carboxylméthyltransférase. | Papaharalambus, C., et al. 2005. J Biol Chem. 280: 18790-6. PMID: 15647276
- Mécanisme cinétique de la protéine isoprénylée méthyltransférase. | Shi, YQ. and Rando, RR. 1992. J Biol Chem. 267: 9547-51. PMID: 1577795
- Analogues de la farnésylcystéine substitués par des amides comme inhibiteurs de l'isoprénylcystéine carboxylméthyltransférase humaine. | Donelson, JL., et al. 2006. Bioorg Med Chem Lett. 16: 4420-3. PMID: 16777414
- La N-acétyl-S-farnésyl-L-cystéine topique inhibe l'inflammation cutanée chez la souris et, contrairement à la dexaméthasone, ses effets sont limités au site d'application. | Gordon, JS., et al. 2008. J Invest Dermatol. 128: 643-54. PMID: 17882268
- La méthylation carboxyle des protéines rap1 des plaquettes est stimulée par la guanosine 5'-(3-O-thio)triphosphate. | Huzoor-Akbar, ., et al. 1991. J Biol Chem. 266: 4387-91. PMID: 1900293
- Réactions de méthylation et de déméthylation des protéines de liaison au nucléotide guanine des segments externes des bâtonnets rétiniens. | Pérez-Sala, D., et al. 1991. Proc Natl Acad Sci U S A. 88: 3043-6. PMID: 1901651
- Identification de l'unité de reconnaissance pour la méthylation des protéines G. | Tan, EW., et al. 1991. J Biol Chem. 266: 10719-22. PMID: 1904056
- Effets des analogues de la farnésylcystéine sur la méthylation carboxyle des protéines et la transduction des signaux. | Volker, C., et al. 1991. J Biol Chem. 266: 21515-22. PMID: 1939182
- Analogues de la prénylcystéine substitués par des lipides et du soufre en tant qu'inhibiteurs de l'Icmt humain. | Bergman, JA., et al. 2011. Bioorg Med Chem Lett. 21: 5616-9. PMID: 21782433
- La N-acétyl-S-farnésyl-l-cystéine supprime la production de chimiokines par les cellules endothéliales microvasculaires dermiques humaines. | Adhami, K., et al. 2012. Exp Dermatol. 21: 700-5. PMID: 22897577
- Études mécanistes sur la méthyltransférase de la protéine isoprénylée plaquettaire humaine: les analogues de la farnésylcystéine bloquent l'agrégation plaquettaire sans inhiber la méthyltransférase. | Ma, YT., et al. 1994. Biochemistry. 33: 5414-20. PMID: 8180165
- Les analogues de la farnésyl-L-cystéine peuvent inhiber ou déclencher la libération de superoxyde par les neutrophiles humains. | Ding, J., et al. 1994. J Biol Chem. 269: 16837-44. PMID: 8207006
- Un analogue de la protéine prénylcystéine inhibe la transduction du signal médiée par les récepteurs agonistes dans les plaquettes humaines. | Huzoor-Akbar, ., et al. 1993. Proc Natl Acad Sci U S A. 90: 868-72. PMID: 8430099
- Carboxyl méthylation des protéines liées à Ras pendant la transduction du signal dans les neutrophiles. | Philips, MR., et al. 1993. Science. 259: 977-80. PMID: 8438158
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
N-Acetyl-S-farnesyl-L-cysteine (AFC), 5 mg | sc-200839 | 5 mg | $88.00 | |||
N-Acetyl-S-farnesyl-L-cysteine (AFC), 25 mg | sc-200839A | 25 mg | $230.00 |
