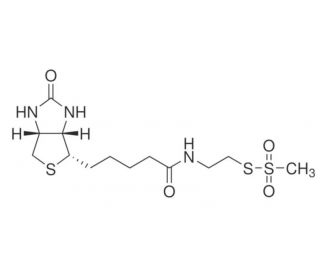
MTSEA Biotin (CAS 162758-04-5)
ACCÈS RAPIDE AUX LIENS
La biotine MTSEA est un composé thiol biotinylé très polyvalent, largement utilisé dans les domaines de la biochimie et de la biologie moléculaire. Sa caractéristique exceptionnelle est sa capacité à se lier de manière covalente à divers substrats, ce qui la rend utile pour de nombreuses applications. Le NBME est largement utilisé dans la modification des protéines, la synthèse des peptides, le marquage de l'ADN/ARN et les essais enzymatiques. Dans la recherche scientifique, la biotine MTSEA a joué un rôle essentiel dans les recherches en protéomique et en biologie moléculaire. Ses applications couvrent un large éventail, allant de la modification des protéines, des peptides et des acides nucléiques au marquage des enzymes et d'autres molécules pour divers essais. En outre, la biotine MTSEA a permis l'étude des interactions protéine-protéine, l'exploration de la structure et de la fonction des protéines, ainsi que des recherches sur la structure et la fonction de l'ADN et de l'ARN. L'action du MTSEA Biotine est assurée par sa liaison covalente spécifique à divers substrats. Le groupement biotine du NBME se lie sélectivement aux domaines de liaison à la biotine des protéines et d'autres molécules, tandis que le groupement thiol se lie aux groupes sulfhydryl présents dans les protéines et d'autres molécules. Il est important de noter que ce processus de liaison est réversible, ce qui permet d'éliminer la biotine MTSEA du substrat à l'aide de méthodes chimiques ou enzymatiques.
MTSEA Biotin (CAS 162758-04-5) Références
- Cartographie du site de liaison agoniste du récepteur GABAA: preuve de l'existence d'un brin bêta. | Boileau, AJ., et al. 1999. J Neurosci. 19: 4847-54. PMID: 10366619
- Structure et dynamique de la poche de liaison du GABA: Une fente étroite qui se resserre lors de l'activation. | Wagner, DA. and Czajkowski, C. 2001. J Neurosci. 21: 67-74. PMID: 11150321
- Étude de l'expression de surface du Na+/Pi-cotransporteur rénal de type IIa dans les ovocytes de Xenopus laevis. | Traebert, M., et al. 2001. J Membr Biol. 180: 83-90. PMID: 11284206
- Déterminants de la potentialisation par le zinc de la sous-unité alpha4 des récepteurs nicotiniques neuronaux. | Hsiao, B., et al. 2006. Mol Pharmacol. 69: 27-36. PMID: 16189299
- Changements structurels induits par les agonistes, les antagonistes et les benzodiazépines dans la région alpha1 Met113-Leu132 du récepteur GABAA. | Kloda, JH. and Czajkowski, C. 2007. Mol Pharmacol. 71: 483-93. PMID: 17108261
- Preuve directe que deux cystéines du transporteur de dopamine forment une liaison disulfure. | Chen, R., et al. 2007. Mol Cell Biochem. 298: 41-8. PMID: 17131045
- Surveillance individuelle des changements induits par les ligands dans la structure du récepteur GABAA au niveau des interfaces du site de liaison des benzodiazépines et du site de non-liaison. | Sharkey, LM. and Czajkowski, C. 2008. Mol Pharmacol. 74: 203-12. PMID: 18424553
- L'interface alpha+bêta- du récepteur GABAA: une nouvelle cible pour les médicaments sélectifs de sous-type. | Ramerstorfer, J., et al. 2011. J Neurosci. 31: 870-7. PMID: 21248110
- Le rôle de ERp44 dans la maturation de la protéine de transport de la sérotonine. | Freyaldenhoven, S., et al. 2012. J Biol Chem. 287: 17801-17811. PMID: 22451649
- Cartographie des résidus importants sur le plan fonctionnel dans le cotransporteur Na+/Dicarboxylate, NaDC1. | Colas, C., et al. 2017. Biochemistry. 56: 4432-4441. PMID: 28731330
- Les résidus du huitième domaine transmembranaire du transporteur de folate couplé au proton (SLC46A1) jouent un rôle important dans la définition de la voie de translocation aqueuse et dans la liaison du substrat de folate. | Aluri, S., et al. 2017. Biochim Biophys Acta Biomembr. 1859: 2193-2202. PMID: 28802835
- L'accessibilité à la cystéine substituée et la réticulation identifient une fente exofaciale dans les 7ème et 8ème hélices du transporteur de folate couplé au proton (SLC46A1). | Aluri, S., et al. 2018. Am J Physiol Cell Physiol. 314: C289-C296. PMID: 29167151
- Substitutions qui verrouillent et déverrouillent le transporteur de folate couplé au proton (PCFT-SLC46A1) dans une conformation ouverte vers l'intérieur. | Aluri, S., et al. 2019. J Biol Chem. 294: 7245-7258. PMID: 30858177
- Système de détection sélectif et sensible de la modification de l'ARN par la 4-thiouridine. | Sugio, Y., et al. 2023. RNA. 29: 241-251. PMID: 36411056
- Détermination de la topologie de la boucle externe du transporteur de sérotonine par marquage chimique dirigé. | Chen, JG., et al. 1998. J Biol Chem. 273: 12675-81. PMID: 9575231
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
MTSEA Biotin, 10 mg | sc-221960 | 10 mg | $213.00 |
