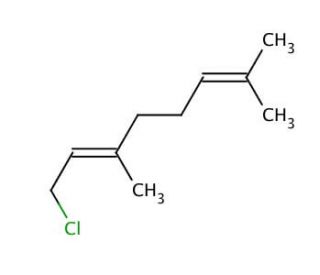
Structure moléculaire de Geranyl chloride, Numéro CAS: 5389-87-7
Geranyl chloride (CAS 5389-87-7)
Noms alternatifs:
trans-1-Chloro-3,7-dimethyl-2,6-octadiene
Application(s):
Geranyl chloride est un réactif de synthèse polyvalent
Numéro CAS:
5389-87-7
Pureté:
95%
Masse Moléculaire:
172.69
Formule Moléculaire:
C10H17Cl
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le chlorure de géranyle sert de substrat dans diverses réactions de synthèse organique. Il sert de précurseur dans la production de terpènes et de terpénoïdes. Le chlorure de géranyle subit des réactions de substitution nucléophile, permettant l'introduction de groupes fonctionnels et la formation de nouvelles liaisons carbone-carbone. Son mécanisme d'action implique la participation à des réactions de substitution aromatique électrophile, permettant la fixation du chlorure de géranyle à des anneaux aromatiques. Le chlorure de géranyle joue un rôle dans la modification des molécules organiques, contribuant à la diversification des structures chimiques dans les applications expérimentales.
Geranyl chloride (CAS 5389-87-7) Références
- Agents antitumoraux II: analogues azotés de l'acide mycophénolique. | Beisler, JA. and Hillery, SS. 1975. J Pharm Sci. 64: 84-7. PMID: 1133712
- Oxydation au permanganate de 1,5,9-triènes: synthèse stéréosélective de fragments contenant du tétrahydrofurane. | Brown, RC., et al. 2002. J Org Chem. 67: 8079-85. PMID: 12423135
- Études de la formation de centres quaternaires tout carbone, en route vers la lyngbyatoxine A. Comparaison des systèmes indole phénylés et 7-substitués. | Tønder, JE., et al. 2004. Org Biomol Chem. 2: 1447-55. PMID: 15136800
- Synthèse du (+)-luzofurane et du (-)-ancistrofurane. | Recsei, C., et al. 2014. J Org Chem. 79: 880-7. PMID: 24437567
- Modulations de réactivité à longue portée dans les dérivés du chlorure de géranyle. | Reardon, MB., et al. 2016. J Org Chem. 81: 10964-10974. PMID: 27704824
- Synthèse bioinspirée de triterpénoïdes onoceranes pentacycliques. | Bartels, F., et al. 2017. Chem Sci. 8: 8285-8290. PMID: 29619174
- Une odeur de rose semblable à celle de l'homme grâce à un nez bioélectronique à base de nanodisques et de récepteurs olfactifs. | Lee, M., et al. 2018. Sci Rep. 8: 13945. PMID: 30224633
- Synthétase de farnésyl pyrophosphate. Études mécanistiques de la réaction de couplage 1'-4 avec le pyrophosphate de 2-fluorogéranyle. | Poulter, CD., et al. 1978. J Biol Chem. 253: 7227-33. PMID: 701246
- Désamination de la nérylamine et de la géranylamine. | Bunton, C. A., Hachey, D. L., & Leresche, J. P. 1972. he Journal of Organic Chemistry. 37(25): 4036-4039.
- Recherche sur les phéromones d'insectes III: études sur les imitations de phéromones d'alarme de pucerons | LI, Z., WANG, T., ME, E., CHEN, X., ZHU, L., & WANG, S. 1987. Acta Chimica Sinica. 45(11): 1124.
- Réexamen de la réduction des chlorures allyliques en oléfines moins substituées par une espèce de chrome de faible valeur en présence d'une source de protons | Omoto, M., Kato, N., Sogon, T., & Mori, A. (. 2001. Tetrahedron Letters. 42(5): 939-941.
- Méthode pratique de préparation d'amines primaires à l'aide de tritylamine | Theodorou, V., Ragoussis, V., Strongilos, A., Zelepos, E., Eleftheriou, A., & Dimitriou, M. 2005. Tetrahedron letters,. 46(8): 1357-1360.
- Pureté, activités antimicrobiennes et évaluations olfactives du géraniol/nerol et de divers de leurs dérivés | Jirovetz, L., Buchbauer, G., Schmidt, E., Stoyanova, A. S., Denkova, Z., Nikolova, R., & Geissler, M. 2007. Journal of Essential Oil Research. 19(3): 288-291.
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Geranyl chloride, 5 g | sc-235244 | 5 g | $81.00 |
