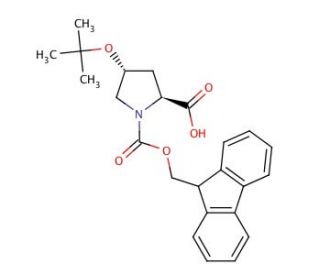
Structure moléculaire de Fmoc-Hyp(tBu)-OH, Numéro CAS: 122996-47-8
Fmoc-Hyp(tBu)-OH (CAS 122996-47-8)
Noms alternatifs:
Fmoc-O-tert-butyl-L-hydroxyproline
Numéro CAS:
122996-47-8
Masse Moléculaire:
409.47
Formule Moléculaire:
C24H27NO5
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Fmoc-Hyp(tBu)-OH est un type de dérivé d'acide aminé utilisé dans la synthèse de peptides. Il a par exemple été utilisé dans la synthèse de peptides destinés à l'étude des interactions protéine-protéine, de la liaison protéine-ligand et de la cinétique enzymatique. Fmoc-Hyp(tBu)-OH sert de groupe protecteur dans la synthèse des peptides. Il est utilisé pour protéger le groupe amine de l'acide aminé contre les réactions indésirables, telles que l'oxydation et l'hydrolyse. Le groupe tert-butyle attaché au groupe hydroxyle sert également à augmenter la stabilité de la molécule, lui permettant de résister à des conditions de réaction plus sévères.
Fmoc-Hyp(tBu)-OH (CAS 122996-47-8) Références
- Synthèse assistée par micro-ondes de lipopeptides triple-hélice, mimétiques du collagène. | Banerjee, J., et al. 2010. Nat Protoc. 5: 39-50. PMID: 20057380
- Les interactions dipôle-dipôle entre brins peuvent stabiliser la triple hélice de collagène. | Shoulders, MD. and Raines, RT. 2011. J Biol Chem. 286: 22905-12. PMID: 21482820
- Une analyse 'conovenomique' du venin de traite de l'escargot Conus textile, chasseur de mollusques: l'importance pharmacologique des modifications post-traductionnelles. | Bergeron, ZL., et al. 2013. Peptides. 49: 145-58. PMID: 24055806
- Photopatterning non covalent de matrices de gélatine à l'aide de peptides mimétiques de collagène en cage. | Li, Y., et al. 2015. Macromol Biosci. 15: 52-62. PMID: 25476588
- Synthèse chimique d'un glycopeptide dérivé de Skp1 pour sonder la glycosylation spécifique des protéines. | Chinoy, ZS., et al. 2015. Chemistry. 21: 11779-87. PMID: 26179871
- Assemblage de nanoparticules et liaison à la gélatine médiés par un peptide mimétique du collagène à triple hélice. | San, BH., et al. 2016. ACS Appl Mater Interfaces. 8: 19907-15. PMID: 27403657
- Synthèse et caractérisation d'un peptide photocléavable de type collagène. | Ornelas, A., et al. 2018. Org Biomol Chem. 16: 1000-1013. PMID: 29345707
- Caractérisation du peptide antimicrobien en épingle à cheveux contenant de l'hydroxyproline EcAMP1-Hyp provenant de graines d'échinochloa (Echinochloa crusgalli L.): Identification structurale et analyse comparative de l'activité antifongique. | Rogozhin, E., et al. 2018. Int J Mol Sci. 19: PMID: 30400225
- Optimisation du domaine de liaison dans un composé dimérique qui dégrade l'expansion d'une répétition r(CUG) dans les cellules. | Benhamou, RI., et al. 2020. J Med Chem. 63: 7827-7839. PMID: 32657583
- Conjugués de chitosane et d'alginate de calcium avec des dérivés d'oligoproline et d'oligohydroxyproline pour une utilisation potentielle en médecine régénérative. | Wasko, J., et al. 2020. Materials (Basel). 13: PMID: 32664253
- Des sondes peptidiques avec des résidus aromatiques Tyr et Phe en position X montrent une haute spécificité pour cibler le collagène dénaturé dans les tissus. | Wei, W., et al. 2020. ACS Omega. 5: 33075-33082. PMID: 33403269
- Conception rationnelle d'un peptide végétal en épingle à cheveux, l'EcAMP1: corrélations structurelles-fonctionnelles pour révéler l'activité antibactérienne et antifongique. | Barashkova, AS., et al. 2022. Molecules. 27: PMID: 35684491
- Synthèse chimique de glycopeptides contenant de l'hydroxyproline arabinosylée et de la tyrosine sulfatée. | van de Sande, JW. and Albada, B. 2023. Org Lett. 25: 1907-1911. PMID: 36917069
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Fmoc-Hyp(tBu)-OH, 5 g | sc-228190 | 5 g | $276.00 |
