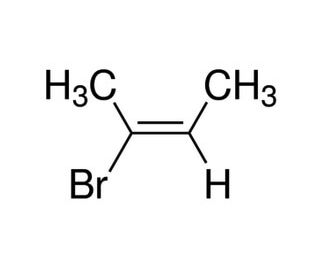
(E)-2-Bromo-2-butene (CAS 3017-71-8)
ACCÈS RAPIDE AUX LIENS
Le (E)-2-bromo-2-butène est un agent alkylant. Son mécanisme d'action implique la capacité de former des liaisons covalentes avec des groupes nucléophiles dans les molécules, en particulier avec les atomes de soufre, d'oxygène et d'azote dans les protéines et les acides nucléiques. Le (E)-2-Bromo-2-Butène peut modifier la structure et la fonction des biomolécules en alkylant des sites spécifiques, ce qui entraîne des changements dans leur activité et leurs interactions. Le mécanisme d'action du (E)-2-Bromo-2-butène implique la substitution d'un atome de brome par un atome d'hydrogène dans la molécule cible, ce qui entraîne la formation d'une nouvelle liaison carbone-carbone. Ce processus peut perturber le fonctionnement normal de la biomolécule, ce qui permet de mieux comprendre le rôle de groupes fonctionnels spécifiques dans les processus biologiques. La réactivité du (E)-2-Bromo-2-butène permet la modification sélective de certaines biomolécules.
(E)-2-Bromo-2-butene (CAS 3017-71-8) Références
- Ligands hémilabiles dans la chimie des organolithes: effets des substituants sur la chélation des ions lithium. | Ramírez, A., et al. 2003. J Am Chem Soc. 125: 15376-87. PMID: 14664582
- Synthèse totale courte et efficace des limonoïdes fraxinellone en utilisant la réaction stéréosélective d'Oshima-Utimoto. | Trudeau, S. and Morken, JP. 2005. Org Lett. 7: 5465-8. PMID: 16288532
- Synthèse concise du squelette néo-clérodane de la teucrolivine A à l'aide d'une cascade de réactions péricycliques. | Arns, S. and Barriault, L. 2006. J Org Chem. 71: 1809-16. PMID: 16496965
- La synthèse permet une révision structurelle du diterpène produit par Mycobacterium tuberculosis, l'edaxadiène. | Spangler, JE., et al. 2010. Chem Sci. 1: 202-205. PMID: 22114734
- Synthèses totales énantiosélectives et configuration absolue de JBIR-02 et Mer-A2026B. | Hoecker, J. and Gademann, K. 2013. Org Lett. 15: 670-3. PMID: 23330661
- Comparaison directe des voies d'élimination du HBr à 3 centres et à 4 centres dans les bromures de vinyle substitués par des méthyles. | Pandit, S., et al. 2016. Phys Chem Chem Phys. 18: 28353-28364. PMID: 27722312
- Synthèse d'alcènes E- et Z-trisubstitués par métathèse croisée catalytique. | Nguyen, TT., et al. 2017. Nature. 552: 347-354. PMID: 29293209
- Synthèse évolutive de la (-)-Rasfonine grâce à une stratégie convergente d'α-Hydroxyméthylation énantiosélective. | Boeckman, RK., et al. 2018. Org Lett. 20: 5062-5065. PMID: 30074398
- Fonctionnalisation radicale d'acides aminés insaturés: synthèse d'acides aminés fluorés, azido-substitués et hydroxylés à chaîne latérale. | Reeve, PAP., et al. 2019. ACS Omega. 4: 10854-10865. PMID: 31460183
- Réactions catalytiques de métathèse croisée permettant d'obtenir des bromures d'alcényle E- et Z-trisubstitués: Champ d'application, applications et perspectives mécanistiques. | Koengeter, T., et al. 2023. J Am Chem Soc. 145: 3774-3785. PMID: 36724200
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
(E)-2-Bromo-2-butene, 5 ml | sc-234855 | 5 ml | $219.00 |
