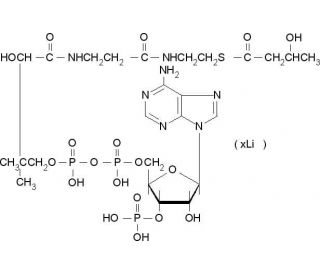
DL-β-Hydroxybutyryl coenzyme A lithium salt (CAS 103404-51-9)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
Le sel de lithium du DL-β-Hydroxybutyryl coenzyme A sert de matériau de départ essentiel pour la synthèse des polyhydroxyalcanoates (PHB) bactériens par l'action des polyhydroxybutyrate (PHB) synthases. Ce composé joue un rôle crucial dans le contexte plus large de la biosynthèse microbienne et de la production de polymères biodégradables, soulignant son importance dans la recherche biotechnologique visant à développer des matériaux durables. Son implication dans le métabolisme des acides gras et la production d'énergie souligne son importance fondamentale dans les voies biochimiques qui sont au cœur des processus cellulaires. Ainsi, le sel de lithium du DL-β-Hydroxybutyryl coenzyme A est non seulement essentiel pour la synthèse du PHB, un biopolymère intéressant pour ses propriétés biodégradables, mais il représente également un nœud clé dans les réseaux métaboliques qui facilitent la conversion des substrats lipidiques en produits biotechnologiques de valeur, offrant ainsi des perspectives pour l'optimisation des stratégies d'ingénierie métabolique en vue d'améliorer l'efficacité de la biosynthèse.
DL-β-Hydroxybutyryl coenzyme A lithium salt (CAS 103404-51-9) Références
- Détection de l'activité de la polyhydroxyalcanoate synthase sur un gel de polyacrylamide. | Sheu, DS., et al. 2009. Anal Biochem. 393: 62-6. PMID: 19527674
- Détection d'intermédiaires covalents et non covalents dans la réaction de polymérisation catalysée par une polyhydroxybutyrate synthase de classe III C149S. | Li, P., et al. 2009. Biochemistry. 48: 9202-11. PMID: 19711985
- Caractérisation de la polyhydroxyalcanoate synthase hautement active de Chromobacterium sp. souche USM2. | Bhubalan, K., et al. 2011. Appl Environ Microbiol. 77: 2926-33. PMID: 21398494
- Analyse LC-MS/MS du coenzyme A et des acyl-coenzyme A thioesters à chaîne courte. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- Décryptage et ingénierie de la production de stéroïdes 23,24-bisnorcholéniques dans le métabolisme des stérols. | Xu, LQ., et al. 2016. Sci Rep. 6: 21928. PMID: 26898409
- Production de polyhydroxyalcanoates (PHA) à partir de déchets synthétiques par Pseudomonas pseudoflava: Analyse de l'activité enzymatique de la PHA synthase de P. pseudoflava et P. palleronii. | Venkateswar Reddy, M., et al. 2017. Bioresour Technol. 234: 99-105. PMID: 28319778
- Optimisation de la surexpression d'une protéine chaperonne de la stéroïde C25 déshydrogénase pour la caractérisation biochimique et biophysique. | Niedzialkowska, E., et al. 2017. Protein Expr Purif. 134: 47-62. PMID: 28343996
- Analyse par chromatographie liquide d'interaction hydrophile et spectrométrie de masse en tandem du malonyl-coenzyme A dans des cultures de cellules de cancer du sein par extraction en phase solide en ligne. | Schriewer, A., et al. 2017. J Sep Sci. 40: 4303-4310. PMID: 28877409
- Caractérisation fonctionnelle d'un nouveau gène, Hc-dhs-28, et son rôle dans la protection de l'hôte après l'infection par Haemonchus contortus par la régulation de la formation de la diapause. | Yang, Y., et al. 2020. Int J Parasitol. 50: 945-957. PMID: 32858035
- L'histone désacétylase 3 associe les mitochondries pour conduire l'inflammation dépendante de l'IL-1β en configurant l'oxydation des acides gras. | Chi, Z., et al. 2020. Mol Cell. 80: 43-58.e7. PMID: 32937100
- Impact de la cétogenèse sur le métabolisme hépatique révélé par la protéomique de la β-hydroxybutyrylation de la lysine. | Koronowski, KB., et al. 2021. Cell Rep. 36: 109487. PMID: 34348140
- L'analyse quantitative des acyl-CoA subcellulaires révèle un métabolisme nucléaire distinct et une propionylation des histones dépendante de l'isoleucine. | Trefely, S., et al. 2022. Mol Cell. 82: 447-462.e6. PMID: 34856123
- Le β-hydroxybutyrate réduit la réintégration de la préférence de place conditionnée à la cocaïne par l'intermédiaire de la CaMKII-α β-hydroxybutyrylation hippocampique. | Li, H., et al. 2022. Cell Rep. 41: 111724. PMID: 36450263
- Méthode cytochimique quantitative pour la mesure de l'activité de la bêta-hydroxyacyl-CoA déshydrogénase dans le muscle cardiaque du rat. | Chambers, DJ., et al. 1982. Histochemistry. 75: 67-76. PMID: 7118583
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
DL-β-Hydroxybutyryl coenzyme A lithium salt, 10 mg | sc-214926 | 10 mg | $410.00 | |||
DL-β-Hydroxybutyryl coenzyme A lithium salt, 25 mg | sc-214926A | 25 mg | $890.00 | |||
DL-β-Hydroxybutyryl coenzyme A lithium salt, 50 mg | sc-214926B | 50 mg | $1795.00 |
