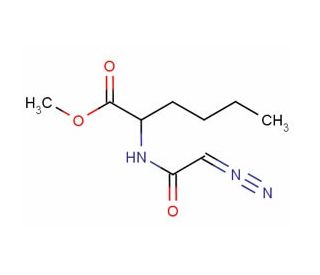
Diazoacetyl-DL-norleucine methyl ester (CAS 7013-09-4)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
L'ester méthylique de diazoacétyl-DL-norleucine, ou DANLE, est un dérivé synthétique de l'acide aminé norleucine qui a suscité un intérêt considérable pour ses applications potentielles dans la recherche scientifique. Sa capacité à inhiber les enzymes qui jouent un rôle dans la synthèse des protéines en a fait un composant important dans de nombreux tests de laboratoire. Les propriétés uniques de l'ester méthylique de diazoacétyl-DL-norleucine ont été explorées dans des études sur la synthèse des protéines dans les cellules eucaryotes et dans des recherches examinant l'impact des inhibiteurs de la synthèse des protéines sur la croissance et le développement des cellules. L'ester méthylique de diazoacétyl-DL-norleucine est également utilisé dans les études sur l'expression des gènes et les effets de l'expression des gènes sur la croissance et la maturation des cellules. Le mécanisme exact par lequel l'ester méthylique de diazoacétyl-DL-norleucine agit n'est pas entièrement connu. Néanmoins, on pense que l'ester méthylique de diazoacétyl-DL-norleucine entrave les enzymes impliquées dans la synthèse des protéines en se fixant sur le site actif de l'enzyme, empêchant ainsi le substrat de se lier. En outre, il est suggéré que l'ester méthylique de diazoacétyl-DL-norleucine pourrait interagir avec d'autres enzymes impliquées dans la synthèse des protéines, telles que celles qui participent à la traduction de l'ARNm.
Diazoacetyl-DL-norleucine methyl ester (CAS 7013-09-4) Références
- Structure et fonction des protéases acides. V. Études comparatives sur l'inhibition spécifique des protéases acides par l'ester méthylique de diazoacétyl-DL-norleucine, le 1,2-époxy-3-(p-nitrophénoxy) propane et la pepstatine. | Takahashi, K. and Chang, WJ. 1976. J Biochem. 80: 497-506. PMID: 10290
- Inhibition spécifique des protéases acides du cerveau, du rein, du muscle squelettique et des plantes insectivores par l'ester méthylique de diazoacétyl-DL-norleucine et par la pepstatine. | Takahashi, K., et al. 1974. J Biochem. 76: 897-9. PMID: 4436292
- Structure et fonction des protéases acides. Inactivation spécifique d'une protéase acide de Rhizopus chinensis par l'ester méthylique de diazoacétyl-DL-norleucine. | Mizobe, F., et al. 1973. J Biochem. 73: 61-8. PMID: 4570372
- Un peptide de site actif de la pepsine C. | Kay, J. and Ryle, AP. 1971. Biochem J. 123: 75-82. PMID: 4942834
- Activité protéasique associée à la perte d'adhésivité dans le tératocarcinome de la souris. | Meyer, JT., et al. 1983. Exp Cell Res. 143: 63-70. PMID: 6337856
- Purification et caractérisation des pepsinogènes et des pepsines de l'ours noir asiatique, et détermination de la séquence d'acides aminés des 60 résidus NH2-terminaux du principal pepsinogène. | Kageyama, T., et al. 1983. J Biochem. 94: 1557-67. PMID: 6418734
- Études sur les protéinases des organes digestifs de la sardine. II. Purification et caractérisation de deux protéinases acides de l'estomac. | Noda, M. and Murakami, K. 1981. Biochim Biophys Acta. 658: 27-34. PMID: 6783105
- Protéinase acide de type cathepsine D de la muqueuse gastrique humaine. Purification et caractérisation. | Kageyama, T. and Takahashi, K. 1980. J Biochem. 87: 725-35. PMID: 6993448
- Purification et propriétés de la protéinase A de la levure. | Meussdoerffer, F., et al. 1980. J Biol Chem. 255: 12087-93. PMID: 7002931
- Structure et fonction des protéases acides. IX. Isolement et séquences d'acides aminés des peptides contenant les résidus aspartyl du site actif réagissant avec l'ester méthylique de diazoacétyl-DL-norleucine et le 1,2-époxy-3-(p-nitrophenoxy)propane dans la protéase acide de Rhizopus chinensis. | Nakamura, S. and Takahashi, K. 1978. J Biochem. 84: 1593-600. PMID: 739006
- Caractérisation d'une protéinase acide thermostable insensible à la pepstatine provenant d'un Bacillus sp. | Prescott, M., et al. 1995. Int J Biochem Cell Biol. 27: 729-39. PMID: 7648429
- Protéinase aspartique insensible à la pepstatine d'un Bacillus sp. thermophile. | Toogood, HS., et al. 1995. Biochem J. 307 (Pt 3): 783-9. PMID: 7741709
- Purification et caractérisation de la kumamolysine, une nouvelle carboxylprotéinase thermostable insensible à la pepstatine provenant de Bacillus novosp. MN-32. | Murao, S., et al. 1993. J Biol Chem. 268: 349-55. PMID: 8416942
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Diazoacetyl-DL-norleucine methyl ester, 250 mg | sc-294298 | 250 mg | $104.00 | |||
Diazoacetyl-DL-norleucine methyl ester, 1 g | sc-294298A | 1 g | $208.00 |
