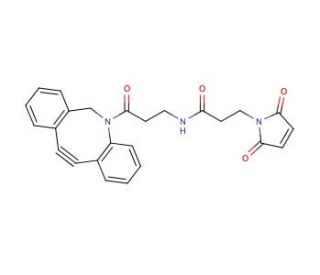
DBCO-maleimide
ACCÈS RAPIDE AUX LIENS
Le DBCO-maléimide est un lien chimique spécialisé qui intègre les propriétés uniques du dibenzocyclooctyne (DBCO) et la réactivité d'un groupe maléimide, ce qui en fait un outil puissant dans le domaine de la bioconjugaison, en particulier dans les applications de la chimie bioorthogonale. Le composant DBCO est réputé pour sa capacité à participer à la cycloaddition alcyne-azide promue par la souche (SPAAC), une réaction de chimie click sans cuivre qui facilite l'assemblage rapide et spécifique de molécules. Cette réaction est particulièrement utile dans les environnements biologiques sensibles où l'introduction de cuivre pourrait avoir des effets cytotoxiques. La réaction SPAAC permet une conjugaison efficace et propre de molécules azotées dans des conditions ambiantes, ce qui renforce l'utilité de cet outil pour le marquage des cellules vivantes et l'étude des processus biologiques dynamiques. À l'autre extrémité de la molécule, le groupe maléimide réagit spécifiquement aux groupes thiols, tels que ceux que l'on trouve sur les résidus de cystéine dans les protéines. Cela permet une fixation précise et stable des protéines, des peptides ou d'autres composés contenant des thiols, formant des liaisons thioéther robustes sans altérer la structure ou la fonction globale de la biomolécule. La double fonctionnalité du DBCO-maléimide en a fait un élément précieux dans la recherche axée sur l'ingénierie des protéines, le développement d'outils de diagnostic et l'assemblage d'architectures moléculaires complexes. La capacité de ce linker à relier des molécules avec une grande spécificité dans des conditions physiologiques soutient son utilisation répandue dans la création de constructions biomoléculaires sophistiquées pour des applications de recherche avancée.
DBCO-maleimide Références
- Marquage spécifique des protéines pour la microscopie électronique. | Dambacher, CM. and Lander, GC. 2015. J Struct Biol. 192: 151-8. PMID: 26409249
- Marquage d'anticorps par photoconjugaison covalente de domaines Z fonctionnalisés pour des réactions de cycloaddition alcyne-azide. | Perols, A., et al. 2015. Chembiochem. 16: 2522-9. PMID: 26417902
- Formation efficace d'hybrides protéine-ADN spécifiques d'un site à l'aide de la chimie Click sans cuivre. | Mukhortava, A. and Schlierf, M. 2016. Bioconjug Chem. 27: 1559-63. PMID: 27322198
- Délivrance ciblée de cyclotides par conjugaison à un nanocorps. | Kwon, S., et al. 2018. ACS Chem Biol. 13: 2973-2980. PMID: 30248263
- Stratégies de multiconjugaison faciles et spécifiques à un site dans les protéines recombinantes produites dans des bactéries. | Merten, H., et al. 2019. Methods Mol Biol. 2033: 253-273. PMID: 31332759
- Méthodes bioorthogonales de conjugaison protéine-ADN pour la spectroscopie de force. | Synakewicz, M., et al. 2019. Sci Rep. 9: 13820. PMID: 31554828
- Encapsulation de points quantiques dans des micelles de lipides-PEG et bioconjugaison ultérieure par chimie Click sans cuivre. | Saeboe, AM., et al. 2020. Methods Mol Biol. 2135: 95-108. PMID: 32246330
- Stratégies d'anticorps conjugués à des oligonucléotides pour l'immunocoloration cyclique. | Jones, JA., et al. 2021. Sci Rep. 11: 23844. PMID: 34903759
- Livraison de nanodots de carbone ciblés sur les récepteurs grâce à la mise en cage de polymères et à l'attachement du ligand LRP1 soutenu par la chimie Click. | Zhang, F., et al. 2023. Polymers (Basel). 15: PMID: 37896282
- Conjugaison de l'hémoglobine et de l'albumine par cycloaddition azide-alcyne favorisée par la souche. | Lee, C., et al. 2024. Chembiochem. e202400206. PMID: 38837740
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
DBCO-maleimide, 1 mg | sc-397264 | 1 mg | $17.00 | |||
DBCO-maleimide, 5 mg | sc-397264A | 5 mg | $81.00 |
