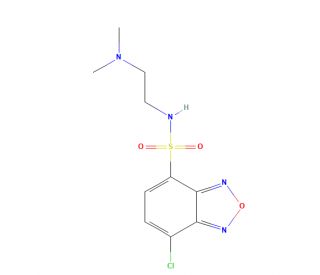
DAABD-Cl (CAS 664985-43-7)
ACCÈS RAPIDE AUX LIENS
Le DAABD-Cl est un composé organique polyvalent utilisé à la fois comme réactif dans la synthèse organique et comme outil de recherche précieux dans les études scientifiques. Ce solide cristallin blanc est soluble dans divers solvants organiques, notamment l'éthanol, le diméthylformamide et le sulfoxyde de diméthyle. Dans le domaine de la synthèse organique, le DAABD-Cl trouve de multiples applications. Il est utilisé dans la synthèse de sulfonamides, d'amines et d'amides, contribuant ainsi à la préparation de divers composés. En outre, le DAABD-Cl sert de catalyseur dans la synthèse de composés hétérocycliques tels que les quinolones, les pyridines et les thiazoles. En outre, le DAABD-Cl est un outil de recherche précieux pour l'étude des effets biochimiques et physiologiques. Il a été largement utilisé pour étudier l'impact de divers médicaments sur le système nerveux et les effets des hormones sur le corps. En outre, le DAABD-Cl a joué un rôle dans l'examen de l'influence des polluants environnementaux et des toxines sur l'organisme, ainsi que des effets de différents médicaments sur les systèmes immunitaire et cardiovasculaire. Le mécanisme d'action précis de DAABD-Cl n'est pas encore totalement élucidé, mais on suppose qu'il fonctionne comme un inhibiteur d'enzymes, bloquant l'activité d'enzymes spécifiques dans l'organisme. En outre, DAABD-Cl a démontré des interactions avec certaines protéines, ce qui pourrait conduire à l'inhibition de processus cellulaires spécifiques. En outre, le DAABD-Cl présente une gamme variée d'effets biochimiques et physiologiques. Il peut inhiber l'activité d'enzymes, y compris les enzymes du cytochrome P450 impliquées dans le métabolisme des médicaments et des produits chimiques. En outre, il a démontré sa capacité à entraver l'activité de protéines telles que la cyclooxygénase-2, responsable de la production de médiateurs inflammatoires. En outre, il a été observé que le DAABD-Cl entrave l'activité d'hormones telles que le cortisol, pour la régulation de la réponse au stress.
DAABD-Cl (CAS 664985-43-7) Références
- Réactifs de dérivatisation fluorogènes adaptés à l'isolement et à l'identification des protéines contenant de la cystéine par chromatographie liquide à haute performance et spectrométrie de masse en tandem. | Masuda, M., et al. 2004. Anal Chem. 76: 728-35. PMID: 14750869
- Une méthode améliorée pour les études protéomiques chez C. elegans par dérivatisation fluorogène, isolation HPLC, digestion enzymatique et identification par chromatographie liquide et spectrométrie de masse en tandem. | Masuda, M., et al. 2005. Biomed Chromatogr. 19: 556-60. PMID: 15654727
- Synthèse et évaluation de réactifs fluorogènes pour la détection simultanée de peptides et de protéines par HPLC dans deux échantillons différents. | Saimaru, H., et al. 2006. Biomed Chromatogr. 20: 576-84. PMID: 16779782
- Existence de thiols de faible poids moléculaire chez Caenorhabditis elegans démontrée par la détection HPLC-fluorescène utilisant le 7-chloro-N-[2-(diméthylamino)éthyl]-2,1,3-benzoxadiazole-4-sulfonamide. | Asamoto, H., et al. 2007. Biomed Chromatogr. 21: 999-1004. PMID: 17516464
- Une méthode protéomique révélant les protéines liées à la maladie dans les foies de modèles de souris infectées par l'hépatite. | Ichibangase, T., et al. 2007. J Proteome Res. 6: 2841-9. PMID: 17559251
- Application d'une méthode protéomique améliorée, la dérivatisation fluorogénique - chromatographie liquide - spectrométrie de masse en tandem, à l'analyse différentielle des protéines dans de petites régions du cerveau de la souris. | Asamoto, H., et al. 2008. J Chromatogr A. 1208: 147-55. PMID: 18814880
- Limitation de la colonne d'immunoaffinité pour l'élimination des protéines abondantes du plasma dans la protéomique quantitative du plasma. | Ichibangase, T., et al. 2009. Biomed Chromatogr. 23: 480-7. PMID: 19039805
- Synthèse et évaluation d'un réactif fluorogène pour les études protéomiques: 7-fluoro-N-[2-(diméthylamino)éthyl]-2,1,3-benzoxadiazole-4-sulfonamide (DAABD-F). | Koshiyama, A. and Imai, K. 2010. Analyst. 135: 2119-24. PMID: 20539882
- Méthode FD-LC-MS/MS pour déterminer l'expression des protéines et élucider les événements biochimiques dans les tissus et les cellules. | Ichibangase, T. and Imai, K. 2012. Biol Pharm Bull. 35: 1393-400. PMID: 22975486
- Analyse protéomique complète par dérivation fluorogénique, chromatographie liquide et spectrométrie de masse en tandem de cellules cancéreuses colorectales afin d'identifier des candidats biomarqueurs. | Koshiyama, A., et al. 2013. Biomed Chromatogr. 27: 440-50. PMID: 22991145
- Séparation chromatographique efficace de protéines intactes dérivées avec un réactif fluorogène pour l'analyse protéomique. | Ichibangase, T., et al. 2013. Biomed Chromatogr. 27: 1520-3. PMID: 23813469
- Analyse complète et temporelle des protéines sécrétées dans le milieu de l'hépatocyte humain exposé à l'IL-6. | Nakata, K., et al. 2014. Biomed Chromatogr. 28: 742-50. PMID: 24861739
- Amélioration de la séparation des protéines intactes dérivées du fluorogène avec une résolution et une efficacité élevées à l'aide d'un système de chromatographie liquide en phase inversée. | Ichibangase, T., et al. 2014. Biomed Chromatogr. 28: 862-7. PMID: 24861755
- Quantification des protéines plasmatiques du cheval modifiées par la xylazine à l'aide de la dérivatisation fluorogénique - chromatographie liquide - spectrométrie de masse en tandem. | Mori, M., et al. 2015. J Equine Sci. 26: 141-6. PMID: 26858580
- Aperçu structurel et fonctionnel de la S-thiolation des albumines sériques humaines. | Nakashima, F., et al. 2018. Sci Rep. 8: 932. PMID: 29343798
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
DAABD-Cl, 100 mg | sc-489828 | 100 mg | $443.00 |
