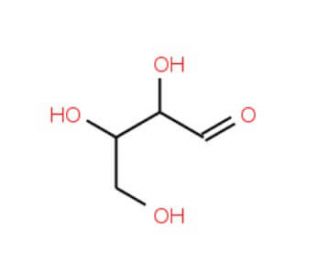
D-Threose (CAS 95-43-2)
QUICK LINKS
D-Threose is a monosaccharide that plays a role in the field of organic chemistry and biochemistry, particularly in the study of carbohydrate structure and metabolism. In synthetic chemistry, it serves as a building block for the assembly of more complex sugar molecules and for the synthesis of analogs that mimic natural sugars in biological systems. Researchers also use D-Threose in chiral pool synthesis due to its enantiomeric purity, which is valuable for producing stereospecific compounds. In the study of prebiotic chemistry, D-Threose is of interest because of its potential role in the origins of life, where it may have been involved in the formation of the first biomolecules. Additionally, this sugar is utilized in the development of glycoconjugates for research in glycoscience, including the exploration of carbohydrate-protein interactions. The simple structure of D-Threose allows for modifications that can facilitate the study of specific biochemical pathways and processes.
D-Threose (CAS 95-43-2) References
- Structure and mechanism of formation of human lens fluorophore LM-1. Relationship to vesperlysine A and the advanced Maillard reaction in aging, diabetes, and cataractogenesis. | Tessier, F., et al. 1999. J Biol Chem. 274: 20796-804. PMID: 10409619
- L-Xylose dehydrogenase in baker's yeast. | UEHARA, K. and TAKEDA, M. 1962. J Biochem. 52: 461-3. PMID: 13995171
- Isolation, purification and characterization of histidino-threosidine, a novel Maillard reaction protein crosslink from threose, lysine and histidine. | Dai, Z., et al. 2007. Arch Biochem Biophys. 463: 78-88. PMID: 17466255
- Inhibitory effects of Terminalia chebula extract on glycation and endothelial cell adhesion. | Lee, HS., et al. 2011. Planta Med. 77: 1060-7. PMID: 21308613
- Computational study of mutarotation in erythrose and threose. | Alkorta, I. and Popelier, PL. 2011. Carbohydr Res. 346: 2933-9. PMID: 22063503
- Enhancement of cyclopamine via conjugation with nonmetabolic sugars. | Goff, RD. and Thorson, JS. 2012. Org Lett. 14: 2454-7. PMID: 22540932
- Conformational study of the open-chain and furanose structures of D-erythrose and D-threose. | Azofra, LM., et al. 2012. Carbohydr Res. 358: 96-105. PMID: 22841585
- Theoretical study of the mutarotation of erythrose and threose: acid catalysis. | Azofra, LM., et al. 2013. Carbohydr Res. 372: 1-8. PMID: 23501397
- Characterization of erythrose reductases from filamentous fungi. | Jovanović, B., et al. 2013. AMB Express. 3: 43. PMID: 23924507
- Asymmetric assembly of aldose carbohydrates from formaldehyde and glycolaldehyde by tandem biocatalytic aldol reactions. | Szekrenyi, A., et al. 2015. Nat Chem. 7: 724-9. PMID: 26291944
- TM0416, a Hyperthermophilic Promiscuous Nonphosphorylated Sugar Isomerase, Catalyzes Various C5 and C6 Epimerization Reactions. | Shin, SM., et al. 2017. Appl Environ Microbiol. 83: PMID: 28258150
- Indium- and Zinc-Mediated Acyloxyallylation of Protected and Unprotected Aldotetroses-Revealing a Pronounced Diastereodivergence and a Fundamental Difference in the Performance of the Mediating Metal. | Draskovits, M., et al. 2018. J Org Chem. 83: 2647-2659. PMID: 29369620
- Methods for enzymatic and colorimetric determinations of D-erythrulose (D-tetrulose). | Morii, K., et al. 1985. Anal Biochem. 151: 188-91. PMID: 4091279
- Studies on L-threose as substrate for aldose reductase: a possible role in preventing protein glycation. | Devamanoharan, PS. and Varma, SD. 1996. Mol Cell Biochem. 159: 123-7. PMID: 8858562
Ordering Information
| Product Name | Catalog # | UNIT | Price | Qty | FAVORITES | |
D-Threose, 250 mg | sc-285394 | 250 mg | $272.00 | |||
D-Threose, 500 mg | sc-285394A | 500 mg | $578.00 |
