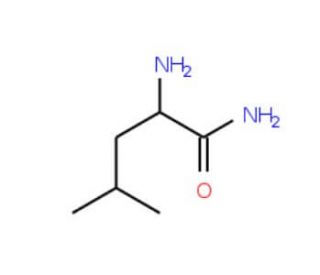
D-Leucine amide (CAS 15893-47-7)
ACCÈS RAPIDE AUX LIENS
La D-Leucine amide est utilisée en chimie biochimique, en particulier dans les études portant sur la structure et la stabilité des peptides. L'amide de D-Leucine joue un rôle essentiel dans l'exploration des propriétés des peptides qui incorporent des acides aminés D, ce qui peut avoir des implications pour la compréhension du repliement et du mauvais repliement des protéines. En enzymologie, la D-Leucine amide sert de substrat ou d'inhibiteur dans des essais conçus pour caractériser la spécificité et le mécanisme d'action des peptidases et d'autres enzymes qui interagissent avec les D-aminoacides. Le D-Leucine amide est utilisé dans le développement de matériaux à base de peptides, où l'incorporation d'acides aminés D peut améliorer la stabilité contre la dégradation enzymatique. La D-Leucine amide est étudiée afin de comprendre le rôle des acides aminés D dans la signalisation cellulaire et les processus neurologiques.
D-Leucine amide (CAS 15893-47-7) Références
- Nouveaux développements dans la synthèse des acides aminés naturels et non naturels. | Kamphuis, J., et al. 1992. Ann N Y Acad Sci. 672: 510-27. PMID: 1476387
- Purification, caractérisation, clonage de gènes et séquençage de nucléotides de la D: -stéréospécifique amidase d'acide aminé d'une bactérie du sol: Delftia acidovorans. | Hongpattarakere, T., et al. 2005. J Ind Microbiol Biotechnol. 32: 567-76. PMID: 15959727
- Synthèse organique basée sur la structure d'hybrides d'aéruginosine non naturels en tant qu'inhibiteurs puissants de la thrombine. | Hanessian, S., et al. 2007. Bioorg Med Chem Lett. 17: 3480-5. PMID: 17428662
- Nouvelle méthode enzymatique de synthèse d'acides aminés chiraux par résolution cinétique dynamique d'amides d'acides aminés: utilisation d'amidases d'acides aminés stéréosélectives en présence d'alpha-amino-epsilon-caprolactame racémase. | Yamaguchi, S., et al. 2007. Appl Environ Microbiol. 73: 5370-3. PMID: 17586677
- Les alpha,alpha-aminoacides cycliques comme échafaudages utiles pour la préparation d'antagonistes du récepteur hNK(2). | Sisto, A., et al. 2007. Bioorg Med Chem Lett. 17: 4841-4. PMID: 17604625
- Une nouvelle aminoacide amidase D-stereospécifique d'Ochrobactrum anthropi. | Asano, Y., et al. 1989. Biochem Biophys Res Commun. 162: 470-4. PMID: 2751665
- Propriétés d'une nouvelle aminopeptidase D-stéréospécifique d'Ochrobactrum anthropi. | Asano, Y., et al. 1989. J Biol Chem. 264: 14233-9. PMID: 2760064
- Production biocatalytique de (S)-2-aminobutanamide par une nouvelle d-aminopeptidase de Brucella sp. avec une activité élevée et une énantiosélectivité. | Tang, XL., et al. 2018. J Biotechnol. 266: 20-26. PMID: 29217400
- Microcystines contenant des résidus de tyrosine doublement homologues provenant d'une fleur de Microcystis aeruginosa: Structures et cytotoxicité. | He, H., et al. 2018. J Nat Prod. 81: 1368-1375. PMID: 29847132
- Leucine aminopeptidase bovine-lens. Études cinétiques avec des substrats et des inhibiteurs de type substrat. | Fittkau, S., et al. 1974. Eur J Biochem. 44: 523-8. PMID: 4838681
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
D-Leucine amide, 1 g | sc-285370 | 1 g | $66.00 | |||
D-Leucine amide, 5 g | sc-285370A | 5 g | $275.00 |
