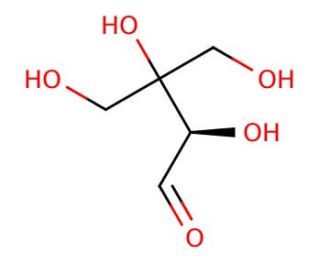
D-Apiose (CAS 639-97-4)
ACCÈS RAPIDE AUX LIENS
Le D-apiose est un sucre impliqué dans la synthèse des polysaccharides de la paroi cellulaire des plantes, en particulier dans la substance pectique apiogalacturonane. Dans le domaine de la recherche, le D-apiose intéresse les biologistes et les chimistes qui étudient son rôle dans la croissance et le développement des plantes, ainsi que sa contribution à l'intégrité structurelle et à la bioactivité des parois cellulaires. En tant que sucre relativement rare, il constitue un modèle pour comprendre la biosynthèse et la fonction des sucres inhabituels dans les plantes. Les recherches sur le D-apiose portent également sur son incorporation dans des produits naturels glycosylés, qui jouent un rôle important dans les mécanismes de défense et de signalisation des plantes. En outre, les chercheurs en chimie de synthèse explorent la synthèse chimique du D-apiose dans le but de créer des analogues de l'apiogalacturonane, qui peuvent être utilisés pour étudier les interactions entre les composants de la paroi cellulaire et d'autres molécules biologiques.
D-Apiose (CAS 639-97-4) Références
- Preuve de l'origine du carbone hydroxyméthyle de la branche D-apiose à partir du carbone 3 de l'acide D-glucuronique. | Kelleher, WJ., et al. 1972. FEBS Lett. 22: 203-204. PMID: 11946597
- Études structurales du polysaccharide pectique de la lentille d'eau Lemna minor L. | Golovchenko, VV., et al. 2002. Phytochemistry. 60: 89-97. PMID: 11985856
- La déplétion des UDP-D-apiose/UDP-D-xylose synthases entraîne une déficience en rhamnogalacturonan-II, un épaississement de la paroi cellulaire et la mort des cellules chez les plantes supérieures. | Ahn, JW., et al. 2006. J Biol Chem. 281: 13708-13716. PMID: 16549428
- Contrôle développemental de la biosynthèse de l'apiogalacturonane et de la production d'UDP-Apiose chez une lentille d'eau. | Longland, JM., et al. 1989. Plant Physiol. 90: 972-6. PMID: 16666907
- Sondage isotopique de la réaction UDP-Apiose/UDP-Xylose Synthase: Preuve d'un mécanisme via une oxydation couplée et un clivage aldol. | Eixelsberger, T., et al. 2017. Angew Chem Int Ed Engl. 56: 2503-2507. PMID: 28102965
- Affectation fonctionnelle de plusieurs voies cataboliques pour le D-apiose. | Carter, MS., et al. 2018. Nat Chem Biol. 14: 696-705. PMID: 29867142
- Profilage des flavonoïdes des parties aériennes de Chenopodium foliosum Asch. (Amaranthaceae). | Kokanova-Nedialkova, Z. and Nedialkov, PT. 2021. Nat Prod Res. 35: 3336-3340. PMID: 31711317
- Décryptage du mécanisme enzymatique de la contraction des anneaux de sucre dans la biosynthèse de l'UDP-apiose. | Savino, S., et al. 2019. Nat Catal. 2: 1115-1123. PMID: 31844840
- La biosynthèse du D-apiose chez Lemna minor. | Picken, JM. and Mendicino, J. 1967. J Biol Chem. 242: 1629-34. PMID: 4290249
- Isolement et caractérisation partielle des apiogalacturonanes de la paroi cellulaire de Lemna minor. | Hart, DA. and Kindel, PK. 1970. Biochem J. 116: 569-79. PMID: 4314131
- D-apiose réductase d'Aerobacter aerogenes. | Neal, DL. and Kindel, PK. 1970. J Bacteriol. 101: 910-5. PMID: 4314545
- Biosynthèse du D-apiose. V. Biosynthèse NAD+-dépendante de l'UDP-apiose et de l'UDP-xylose à partir de l'acide UDP-D-glucuronique avec une préparation enzymatique de Lemna minor L. | Sandermann, H. and Grisebach, H. 1970. Biochim Biophys Acta. 208: 173-80. PMID: 4393018
- Synthèse de 3-C-hydroxyméthyl-1,2-O-isopropylidene- -D-erythrofuranose et de D-apiose. | Ezekiel, AD., et al. 1971. Carbohydr Res. 20: 251-7. PMID: 5152098
- Biosynthèse du D-apiose. IV. Formation de l'UDP-apiose à partir de l'acide UDP-D-glucuronique dans des extraits cellulaires de persil (Apium petroselinum L.) et de Lemna minor. | Sandermann, H., et al. 1968. Biochim Biophys Acta. 165: 550-2. PMID: 5737946
- Biosynthèse du D-apiose dans un système acellulaire à partir de Lemna minor L. | Gustine, DL. and Kindel, PK. 1969. J Biol Chem. 244: 1382-5. PMID: 5767313
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
D-Apiose, 2.5 mg | sc-285338 | 2.5 mg | $277.00 | |||
D-Apiose, 50 mg | sc-285338A | 50 mg | $1746.00 | |||
D-Apiose, 100 mg | sc-285338B | 100 mg | $3339.00 |
