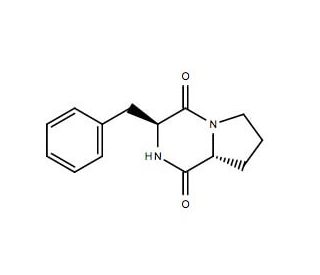
Cyclo(L-Phe-D-Pro)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
Le cyclo(L-Phe-D-Pro) est un composé dipeptidique qui sert d'échafaudage moléculaire dans la chimie des peptides. Il peut jouer un rôle dans la stabilisation de la conformation des peptides et des protéines, en particulier dans la conception et la synthèse de composés bioactifs. Le mécanisme d'action du cyclo(L-Phe-D-Pro) consiste à influencer l'arrangement spatial des résidus d'acides aminés, affectant ainsi la structure et la fonction du peptide ou de la protéine. Cyclo(L-Phe-D-Pro) est utilisé dans des applications visant à explorer l'impact des contraintes conformationnelles sur l'activité biologique des peptides, des protéines et des protéines. Le Cyclo(L-Phe-D-Pro) interagit avec le squelette du peptide, influençant son modèle de pliage et modifiant potentiellement son affinité de liaison ou son activité enzymatique. Le rôle fonctionnel du Cyclo(L-Phe-D-Pro) dans les applications expérimentales réside dans sa capacité à moduler la flexibilité conformationnelle des peptides, contribuant ainsi à l'étude des relations structure-activité des molécules bioactives.
Cyclo(L-Phe-D-Pro) Références
- Dicétopipérazines antimicrobiennes et inhibitrices de biofilms. | de Carvalho, MP. and Abraham, WR. 2012. Curr Med Chem. 19: 3564-77. PMID: 22709011
- Activation de l'acide D-lysergique et synthèse acellulaire de peptides D-lysergiques dans les fractions enzymatiques du champignon ergot Claviceps purpurea. | Keller, U., et al. 1988. Biochemistry. 27: 6164-70. PMID: 2847788
- Potentiel antibactérien des métabolites secondaires des symbiotes bactériens marins indonésiens. | Nofiani, R., et al. 2020. Int J Microbiol. 2020: 8898631. PMID: 32676116
- Calculs d'énergie potentielle sur les rotamères de phénylalanine dans différentes formes de bateaux de dipeptides cycliques contenant de la proline. | Mazza, F., et al. 1988. Int J Pept Protein Res. 31: 157-63. PMID: 3366549
- Dipeptides cycliques: Le paysage biologique et structurel avec un accent particulier sur l'échafaudage anti-cancer à base de proline. | Bojarska, J., et al. 2021. Biomolecules. 11: PMID: 34680148
- Activité antibactérienne de deux métabolites isolés de la bactérie endophyte Bacillus velezensis Ea73 dans Ageratina adenophora. | Ren, Z., et al. 2022. Front Microbiol. 13: 860009. PMID: 35602058
- Extraction de petites molécules à partir de souches de Teredinibacter turnerae isolées à partir de Teredinidae philippins. | Villacorta, JB., et al. 2022. Metabolites. 12: PMID: 36422292
- Identification d'un nouveau métabolite sécrété cyclo(phénylalanyl-prolyl) de Batrachochytrium dendrobatidis et son effet sur Galleria mellonella. | Starr, AM., et al. 2022. BMC Microbiol. 22: 293. PMID: 36482304
- Spiroquinazoline, un nouvel inhibiteur de la substance P avec un nouveau squelette de carbone, isolé d'Aspergillus flavipes. | Barrow, CJ. and Sun, HH. 1994. J Nat Prod. 57: 471-6. PMID: 7517439
- N-Acyl-dicétopipérazines: II. Structure cristalline et conformation de la N-(pyruvoyl)-cyclo-(L-phénylalanyl-D-prolyl) | ANNACALCAGNI, MAZZA, F., POCHETTI, G., ROSSI, D., & LUCENTE, G. 1985. International Journal of Peptide and Protein Research. 26(2): 166-173.
- Effets de l'encombrement stérique et de la stéréochimie sur les taux de formation de dicétopipérazine à partir de N-aminoacyl-2, 2-diméthylthiazolidine-4-carboxamides (amides dipeptidiques Dmt) - un modèle pour un nouveau système de liaison de médicaments. | Suaifan, G. A., Mahon, M. F., Arafat, T., & Threadgill, M. D. 2006. Tetrahedron. 62(48): 11245-11266.
- Les dipeptides cycliques à base de L-proline de Pseudomonas sp.(ABS-36) inhibent les cytokines pro-inflammatoires et atténuent les lésions rénales induites par les cristaux chez les souris | Ahil, S. B., Hira, K., Shaik, A. B., Pal, P. P., Kulkarni, O. P., Araya, H., & Fujimoto, Y. 2019. International Immunopharmacology. 73: 395-404.
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Cyclo(L-Phe-D-Pro), 250 mg | sc-506240 | 250 mg | $333.00 |
