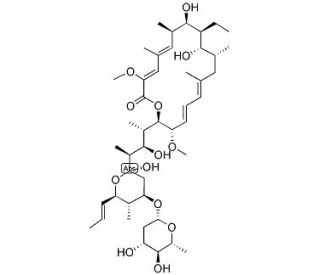
Concanamycin C (CAS 81552-34-3)
Voir les citations produits (4)
ACCÈS RAPIDE AUX LIENS
La concanamycine C, dont le numéro CAS est 81552-34-3, est un composé chimique qui appartient à la classe des concanamycines, un groupe d'antibiotiques macrolides dérivés de la bactérie Streptomyces neyagawaensis. Comme d'autres membres de sa famille, la concanamycine C fonctionne principalement comme un inhibiteur de la H+-ATPase de type vacuolaire (V-ATPase). La V-ATPase est un complexe enzymatique essentiel à l'acidification de divers compartiments intracellulaires, notamment les lysosomes, les endosomes et l'appareil de Golgi. L'inhibition de la V-ATPase par la concanamycine C entraîne une perturbation du processus d'acidification, qui est essentiel pour de nombreuses fonctions cellulaires telles que le tri des protéines, la maturation des précurseurs enzymatiques et la dégradation des déchets cellulaires. Dans le cadre de la recherche, la concanamycine C a été utilisée pour étudier les conséquences physiologiques et biochimiques de l'altération du pH intracellulaire. En bloquant la fonction des V-ATPases, les chercheurs peuvent étudier l'impact sur les processus cellulaires tels que l'autophagie, l'endocytose et la réponse cellulaire au stress environnemental. Ce composé permet d'élucider les mécanismes complexes par lesquels les cellules maintiennent leur pH interne et gèrent le renouvellement de diverses biomolécules, éclairant ainsi les aspects fondamentaux de la biologie cellulaire et de la fonction des organites.
Concanamycin C (CAS 81552-34-3) Références
- Rôle cellulaire de la V-ATPase chez Neurospora crassa: analyse de mutants résistants à la concanamycine ou dépourvus de la sous-unité catalytique A. | Bowman, EJ. and Bowman, BJ. 2000. J Exp Biol. 203: 97-106. PMID: 10600678
- L'interruption de vma-1, le gène codant pour la sous-unité catalytique de la H(+)-ATPase vacuolaire, provoque de graves changements morphologiques chez Neurospora crassa. | Bowman, EJ., et al. 2000. J Biol Chem. 275: 167-76. PMID: 10617601
- Dérivés semi-synthétiques de la concanamycine A et C, en tant qu'inhibiteurs des ATPases de type V et P: études structure-activité et développement de sondes de photo-affinité. | Dröse, S., et al. 2001. Biochemistry. 40: 2816-25. PMID: 11258892
- Un modèle pour l'anneau protéolipidique et le site de liaison à la bafilomycine/concanamycine dans l'ATPase vacuolaire de Neurospora crassa. | Bowman, BJ., et al. 2006. J Biol Chem. 281: 31885-93. PMID: 16912037
- Le mode actif d'excrétion à travers les tissus digestifs est antérieur à l'origine des organes excréteurs. | Andrikou, C., et al. 2019. PLoS Biol. 17: e3000408. PMID: 31356592
- Les relations structure-activité des plécomacrolides naturels et semi-synthétiques suggèrent des voies distinctes pour l'évasion immunitaire du VIH-1 et l'acidification lysosomale dépendante de l'ATPase vacuolaire. | McCauley, M., et al. 2024. J Med Chem. 67: 4483-4495. PMID: 38452116
- Isolement et caractérisation des concanamycines A, B et C. | Kinashi, H., et al. 1984. J Antibiot (Tokyo). 37: 1333-43. PMID: 6511660
- La sécrétion basolatérale de la protéine précurseur de l'amyloïde dans les cellules rénales de l'espèce Madin-Darby est perturbée par des modifications du pH intracellulaire et par l'introduction d'une mutation associée à la maladie d'Alzheimer familiale. | De Strooper, B., et al. 1995. J Biol Chem. 270: 4058-65. PMID: 7876155
- Effet inhibiteur des bafilomycines et concanamycines modifiées sur les adénosinetriphosphatases de type P et V. | Dröse, S., et al. 1993. Biochemistry. 32: 3902-6. PMID: 8385991
- Produits métaboliques des micro-organismes. Partie 265. Prélactones C et B, oligokétides de Streptomyces produisant des concanamycines et des bafilomycines. | Bindseil, et al. 1993. Helvetica chimica acta. 76.1: 150-157.
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Concanamycin C, 100 µg | sc-203006 | 100 µg | $280.00 | |||
Concanamycin C, 500 µg | sc-203006A | 500 µg | $785.00 |
