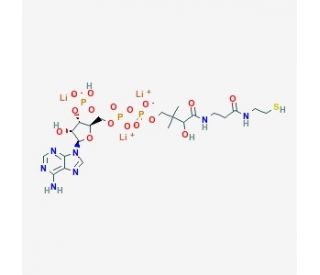
Structure moléculaire de Coenzyme A, Trilithium Salt, Numéro CAS: 18439-24-2
Coenzyme A, Trilithium Salt (CAS 18439-24-2)
Application(s):
Coenzyme A, Trilithium Salt est un cofacteur dans les réactions enzymatiques de transfert d'acétyle.
Numéro CAS:
18439-24-2
Pureté:
≥94%
Masse Moléculaire:
785.33
Formule Moléculaire:
C21H33N7O16P3S•3Li
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le coenzyme A, sel de trilithium (CAT) est un cofacteur dans les réactions enzymatiques de transfert d'acétyle. Il se lie aux sites actifs des enzymes et des protéines, ce qui permet de les activer ou de les inhiber. Il se lie également aux médicaments et aux acides gras, ce qui permet de les métaboliser plus facilement. Le sel trilithium de coenzyme A a été utilisé dans la recherche scientifique pour étudier la structure et la fonction des enzymes et des protéines, pour étudier le mécanisme d'action des médicaments et pour étudier le métabolisme des acides gras.
Coenzyme A, Trilithium Salt (CAS 18439-24-2) Références
- Propionate CoA-transférase de Clostridium propionicum. Clonage du gène et identification du glutamate 324 dans le site actif. | Selmer, T., et al. 2002. Eur J Biochem. 269: 372-80. PMID: 11784332
- Conception, synthèse et test in vitro d'inhibiteurs de l'alpha-méthylacyl-CoA racémase. | Carnell, AJ., et al. 2007. J Med Chem. 50: 2700-7. PMID: 17477519
- Synthèse et caractérisation du cis-4-décénoyl-CoA, du 3-phénylpropionyl-CoA et du 2,6-diméthylheptanoyl-CoA. | Sobhi, HF., et al. 2010. Anal Biochem. 401: 114-24. PMID: 20184857
- FadD19 de Rhodococcus rhodochrous DSM43269, une stéroïde-coenzyme A ligase essentielle pour la dégradation des chaînes latérales des stérols ramifiés en C-24. | Wilbrink, MH., et al. 2011. Appl Environ Microbiol. 77: 4455-64. PMID: 21602385
- Méthode chirale de chromatographie liquide à haute performance et de spectrométrie de masse en tandem pour l'analyse stéréospécifique des enoyl-coenzyme A hydratases/isomérases. | Abdel-Mawgoud, AM., et al. 2013. J Chromatogr A. 1306: 37-43. PMID: 23906801
- Le trifluoroibuprofène inhibe l'α-méthylacyl coenzyme A racémase (AMACR/P504S), réduit la prolifération des cellules cancéreuses et inhibe la croissance tumorale in vivo dans des modèles agressifs de cancer de la prostate. | Festuccia, C., et al. 2014. Anticancer Agents Med Chem. 14: 1031-41. PMID: 24712326
- La capsaïcine, le nonivamide et la trans-pellitorine diminuent l'absorption des acides gras libres sans activation du TRPV1 et augmentent l'activité de l'acétyl-coenzyme A synthétase dans les cellules Caco-2. | Rohm, B., et al. 2015. Food Funct. 6: 173-85. PMID: 25422952
- Sélection de phages assistée par le marquage de protéines spécifiques à un site par la Sfp phosphopantetheinyl transferase catalysée. | Zhao, B., et al. 2015. Methods Mol Biol. 1266: 161-70. PMID: 25560074
- Analyse LC-MS/MS du coenzyme A et des acyl-coenzyme A thioesters à chaîne courte. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- Enzymes impliquées dans la dégradation anaérobie de l'orthophtalate par la bactérie nitrate-réductrice Azoarcus sp. souche PA01. | Junghare, M., et al. 2016. Environ Microbiol. 18: 3175-88. PMID: 27387486
- Multiplexage du test de viabilité basé sur l'estérase fluorogène avec les tests de la luciférase. | Ohgane, K., et al. 2019. MethodsX. 6: 2013-2020. PMID: 31667098
- Dépistage suspect et analyse ciblée des acyl-coenzyme A thioesters dans les cultures bactériennes à l'aide d'un spectromètre de masse tribride à haute résolution. | Cakić, N., et al. 2021. Anal Bioanal Chem. 413: 3599-3610. PMID: 33881564
- Nouveaux inhibiteurs de bisubstrat pour la protéine N-Terminal Acetyltransferase D. | Deng, Y., et al. 2021. J Med Chem. 64: 8263-8271. PMID: 34110812
- L'analyse quantitative des acyl-CoA subcellulaires révèle un métabolisme nucléaire distinct et une propionylation des histones dépendante de l'isoleucine. | Trefely, S., et al. 2022. Mol Cell. 82: 447-462.e6. PMID: 34856123
- Un nouvel analogue du coenzyme A dans la bactérie marine anaérobie Desulfobacula toluolica Tol2T, qui réduit les sulfates. | Bruns, S., et al. 2023. Chembiochem. 24: e202200584. PMID: 36331165
Activateur de:
GLYATL3.Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Coenzyme A, Trilithium Salt, 25 mg | sc-203901A | 25 mg | $161.00 | |||
Coenzyme A, Trilithium Salt, 100 mg | sc-203901 | 100 mg | $372.00 | |||
Coenzyme A, Trilithium Salt, 250 mg | sc-203901B | 250 mg | $510.00 | |||
Coenzyme A, Trilithium Salt, 1 g | sc-203901C | 1 g | $1805.00 |
