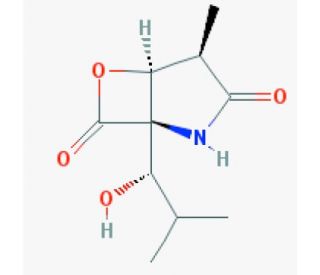
clasto-Lactacystin β-lactone (CAS 155975-72-7)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
La clasto-lactacystine β-lactone (CAS : 155975-72-7) est un produit chimique d'un grand intérêt, principalement en raison de son rôle de précurseur de la lactacystine, une molécule intrigante dans la recherche biochimique en raison de sa capacité à moduler l'activité du protéasome. La clasto-lactacystine β-lactone elle-même, lorsqu'elle est métabolisée, se transforme en lactacystine, qui interagit ensuite avec le protéasome, un complexe protéique responsable de la dégradation des protéines indésirables ou mal repliées dans les cellules. L'action spécifique de la clasto-lactacystine β-lactone implique sa conversion en clasto-lactacystine dihydroxyacide en présence de nucléophiles cellulaires, qui inhibe alors l'activité protéasomale en ciblant spécifiquement les sous-unités β protéolytiques au sein du noyau 20S du protéasome. Cette inhibition est cruciale pour l'étude des mécanismes de dégradation des protéines dans diverses conditions physiologiques, ce qui permet de mieux comprendre la régulation du renouvellement des protéines et ses implications dans les fonctions cellulaires. Les chercheurs utilisent la clasto-Lactacystine β-lactone pour explorer la dynamique de l'inhibition du protéasome et son impact sur l'homéostasie des protéines dans les cellules.
clasto-Lactacystin β-lactone (CAS 155975-72-7) Références
- Croissance neuritique dans les cellules PC12. Distinction des rôles de l'ubiquitylation et de la protéolyse dépendante de l'ubiquitine. | Obin, M., et al. 1999. J Biol Chem. 274: 11789-95. PMID: 10206996
- Une nouvelle voie de synthèse énantiosélective vers des analogues de l'omuralide avec un potentiel de sélectivité des espèces dans l'inhibition du protéasome. | Crane, SN. and Corey, EJ. 2001. Org Lett. 3: 1395-7. PMID: 11348243
- Inhibiteurs du protéasome: des outils de recherche aux médicaments candidats. | Kisselev, AF. and Goldberg, AL. 2001. Chem Biol. 8: 739-58. PMID: 11514224
- Synthèses énantiospécifiques simples des diastéréoisomères C(2) de l'omuralide et du 3-méthylomuralide. | Reddy, LR., et al. 2005. Org Lett. 7: 2703-5. PMID: 15957926
- Inhibition du protéasome par une bêta-lactamine totalement synthétique apparentée au salinosporamide A et à l'omuralide. | Hogan, PC. and Corey, EJ. 2005. J Am Chem Soc. 127: 15386-7. PMID: 16262399
- Prédiction du mécanisme d'action de l'omuralide (clasto-lactacystine bêta-lactone) sur la cathepsine A humaine sur la base d'un modèle structurel du complexe protéasome de levure bêta5/sous-unité PRE2/omuralide. | Aikawa, S., et al. 2006. Biochim Biophys Acta. 1764: 1372-80. PMID: 16870514
- Nouvelle entrée pour les isocyanides convertibles pour la réaction d'Ugi et son application à la synthèse totale formelle stéréocontrôlée de l'omuralide, un inhibiteur du protéasome. | Gilley, CB., et al. 2007. Org Lett. 9: 3631-4. PMID: 17672474
- Synthèses totales stéréospécifiques des inhibiteurs du protéasome omuralide et lactacystine. | Gu, W. and Silverman, RB. 2011. J Org Chem. 76: 8287-93. PMID: 21916437
- Omuralide et vibralactone: les différences dans l'échafaudage de liaison au protéasome - β-lactone-γ-lactame modifient les préférences de la cible. | List, A., et al. 2014. Angew Chem Int Ed Engl. 53: 571-4. PMID: 24285701
- Accès stéréocontrôlé aux δ-lactones-fusées-γ-lactames portant des stéréocentres quaternaires benzyliques angulaires. | Beng, TK., et al. 2022. RSC Adv. 12: 17617-17620. PMID: 35765420
- Inhibition des activités du protéasome et de la modification de la thréonine amino-terminale spécifique à la sous-unité par la lactacystine. | Fenteany, G., et al. 1995. Science. 268: 726-31. PMID: 7732382
- Études mécanistes sur l'inactivation du protéasome par la lactacystine dans des cellules cultivées. | Dick, LR., et al. 1997. J Biol Chem. 272: 182-8. PMID: 8995245
- Synthèse totale et activité biologique de la lactacystine, de l'omuralide et de leurs analogues. | Corey, EJ. and Li, WD. 1999. Chem Pharm Bull (Tokyo). 47: 1-10. PMID: 9987821
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
clasto-Lactacystin β-lactone, 100 µg | sc-202106 | 100 µg | $254.00 |
