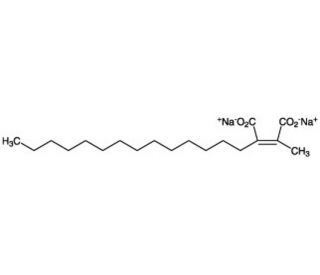
Chaetomellic acid A (CAS 148796-51-4)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
L'acide chétomélique A est un puissant inhibiteur de l'histone désacétylase, qui agit par le biais d'une interaction de liaison spécifique avec le site actif de l'enzyme, empêchant l'élimination des groupes acétyles des protéines histones. Cette action entraîne des niveaux élevés d'acétylation des histones, une modification connue pour détendre la structure de la chromatine et renforcer l'activité transcriptionnelle. La modification de l'état de la chromatine induite par l'acide chaetomellique A a un impact profond sur les profils d'expression des gènes et orchestre une variété de processus cellulaires, ce qui en fait un agent permettant de sonder la dynamique de la modulation épigénétique. En facilitant l'acétylation soutenue des histones, il offre une fenêtre unique sur les complexités moléculaires du remodelage de la chromatine et sur les mécanismes épigénétiques qui sous-tendent la régulation des gènes. Son utilité s'étend à l'élucidation des voies par lesquelles les facteurs épigénétiques influencent la différenciation et la maintenance cellulaires, contribuant ainsi au domaine plus large des études génomiques et à l'exploration du rôle de la chromatine dans la fonctionnalité et le développement cellulaires.
Chaetomellic acid A (CAS 148796-51-4) Références
- Inhibition de la prénylation des protéines par les métabolites du limonène. | Hardcastle, IR., et al. 1999. Biochem Pharmacol. 57: 801-9. PMID: 10075086
- Analyse de l'activité de la farnésyl transférase au cours de la maturation des ovocytes de Xenopus laevis induite par les hormones. | Goalstone, ML. and Sadler, SE. 2000. J Exp Zool. 286: 193-203. PMID: 10617861
- Synthèses efficaces, activités inhibitrices de la farnésyl-protéine transférase humaine et de la levure des acides chaetomelliques et de leurs analogues. | Singh, SB., et al. 2000. Bioorg Med Chem. 8: 571-80. PMID: 10732974
- Synthèse d'inhibiteurs de la protéine farnésyltransférase et de la protéine géranylgeranyltransférase: Accès rapide à l'acide chaetomellique A et à ses analogues. | Ratemi, ES., et al. 1996. J Org Chem. 61: 6296-6301. PMID: 11667470
- Synthèse facile des produits naturels que sont l'acide chaetomellique A et l'acide 1,7(Z)- nonadécadiène-2,3-dicarboxylique. | Kar, A. and Argade, NP. 2002. J Org Chem. 67: 7131-4. PMID: 12354009
- Les inhibiteurs de la farnésyltransférase protéique interfèrent avec la liaison du farnésyl diphosphate par la farnésyltransférase du caoutchouc. | Mau, CJ., et al. 2003. Eur J Biochem. 270: 3939-45. PMID: 14511375
- Synthèse et activité biologique d'analogues du diphosphate d'isopentényle. | Scholte, AA., et al. 2004. Bioorg Med Chem. 12: 763-70. PMID: 14759736
- Synthèse d'analogues mono- et disaccharidiques de la moénomycine et du lipide II pour l'inhibition de l'activité transglycosylase de la protéine 1b de liaison à la pénicilline. | Garneau, S., et al. 2004. Bioorg Med Chem. 12: 6473-94. PMID: 15556765
- L'inhibition de la signalisation Ras/ERK1/2 protège contre les lésions rénales postischémiques. | Sabbatini, M., et al. 2006. Am J Physiol Renal Physiol. 290: F1408-15. PMID: 16434573
- Nouvelle voie d'accès à l'acide chaetomellique A et à ses analogues: découverte fortuite d'un inhibiteur de FTase plus compétent. | Bellesia, F., et al. 2013. Bioorg Med Chem. 21: 348-58. PMID: 23182215
- Effet de l'angiotensine II et de l'inhibition de la voie de signalisation de la petite GTPase Ras sur les changements rénaux précoces dans un modèle murin de néphropathie obstructive. | Rodríguez-Peña, AB., et al. 2014. Biomed Res Int. 2014: 124902. PMID: 25101263
- Les effets de l'administration à long terme de l'acide chaetomellique A sur la fonction rénale et le stress oxydatif dans un modèle de réduction de la masse rénale chez le rat. | Nogueira, A., et al. 2017. Biomed Res Int. 2017: 5125980. PMID: 28326323
- Chaetomella acutiseta produit les acides chaetomelliques A et B qui sont des inhibiteurs réversibles de la farnésyl-protéine transférase. | Lingham, RB., et al. 1993. Appl Microbiol Biotechnol. 40: 370-4. PMID: 7764394
- Synthèse simple et efficace de l'acide chaetomellique A, inhibiteur de la farnésyl-protéinotransférase de la ras. | Argade, NP. and Naik, RH. 1996. Bioorg Med Chem. 4: 881-3. PMID: 8818238
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Chaetomellic acid A, 5 mg | sc-221420 | 5 mg | $48.00 | |||
Chaetomellic acid A, 25 mg | sc-221420A | 25 mg | $255.00 |
