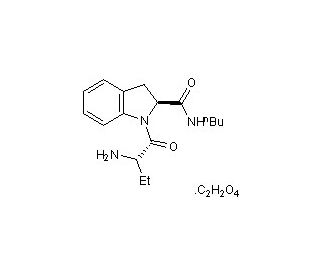
Butabindide oxalate (CAS 185213-03-0)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
L'oxalate de butabindide est un inhibiteur sélectif et puissant de la TPPII (tripeptidyl peptidase II). La TPP II est une enzyme impliquée dans la dégradation des protéines, ciblant spécifiquement les tripeptides pour le clivage, qui joue un rôle dans le système plus large de dégradation et de renouvellement des protéines à l'intérieur des cellules. En inhibant la TPP II, l'oxalate de butabindide peut influencer les voies de traitement et de dégradation des protéines, mettant ainsi en lumière les mécanismes complexes de régulation des protéines intracellulaires. L'inhibition sélective de la TPP II par ce composé le rend précieux pour la recherche biochimique, en particulier dans les études visant à disséquer le rôle de la dégradation des protéines dans la physiologie cellulaire et le maintien de l'homéostasie cellulaire.
Butabindide oxalate (CAS 185213-03-0) Références
- Inhibiteurs de la tripeptidyl peptidase II. 2. Génération du premier nouvel inhibiteur principal de la peptidase inactivant la cholécystokinine-8: une stratégie pour la conception d'inhibiteurs de peptidases. | Ganellin, CR., et al. 2000. J Med Chem. 43: 664-74. PMID: 10691692
- Rôle majeur de la TPPII dans l'élagage des produits de dégradation protéasomale pour la présentation des antigènes de classe I du CMH. | Reits, E., et al. 2004. Immunity. 20: 495-506. PMID: 15084277
- Tripeptidyl peptidase II. Un complexe de protéases oligomériques d'Arabidopsis. | Book, AJ., et al. 2005. Plant Physiol. 138: 1046-57. PMID: 15908606
- L'adjuvant ISCOMATRIX induit une présentation croisée efficace de l'antigène tumoral par les cellules dendritiques grâce à une libération rapide de l'antigène cytosolique et à son traitement par la tripeptidyl peptidase II. | Schnurr, M., et al. 2009. J Immunol. 182: 1253-9. PMID: 19155470
- Le traitement et la présentation croisée des épitopes HLA-A, -B ou -C de NY-ESO-1 ou d'un épitope HLA-A pour Melan-A diffèrent selon le mode d'administration de l'antigène. | Robson, NC., et al. 2010. Blood. 116: 218-25. PMID: 20430956
- Contribution dominante du protéasome et des métalloprotéinases au répertoire peptidique du CMH-I indépendant de la TAP. | Oliveira, CC., et al. 2014. Mol Immunol. 62: 129-36. PMID: 24983205
- Des voies protéolytiques doubles régissent la glycolyse et la compétence immunitaire. | Lu, W., et al. 2014. Cell. 159: 1578-90. PMID: 25525876
- Séparation spatiale des compartiments de traitement et de chargement du CMH de classe I pour la présentation croisée de l'antigène HER2/neu associé à la tumeur par les cellules dendritiques humaines. | Baleeiro, RB., et al. 2015. Oncoimmunology. 4: e1047585. PMID: 26985398
- L'IFN de type I, et non le TNF, est essentiel pour les CTL activés par le di-nucléotide cyclique par une voie de présentation croisée cytosolique. | Lirussi, D., et al. 2017. EBioMedicine. 22: 100-111. PMID: 28754303
- Un criblage à haut contenu identifie TPP1 et Aurora B comme régulateurs du transport mitochondrial axonal. | Shlevkov, E., et al. 2019. Cell Rep. 28: 3224-3237.e5. PMID: 31533043
- Aperçu de la base moléculaire de la stabilité du génome et de la protéostase intacte chez les rats-taupes nus. | Narayan, V., et al. 2021. Adv Exp Med Biol. 1319: 287-314. PMID: 34424521
- Caractérisation et inhibition d'une sérine peptidase inactivant la cholécystokinine. | Rose, C., et al. 1996. Nature. 380: 403-9. PMID: 8602240
- Caractérisation et clonage de la tripeptidyl peptidase II de la drosophile, Drosophila melanogaster. | Renn, SC., et al. 1998. J Biol Chem. 273: 19173-82. PMID: 9668104
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Butabindide oxalate, 10 mg | sc-361130 | 10 mg | $189.00 | |||
Butabindide oxalate, 50 mg | sc-361130A | 50 mg | $770.00 |
