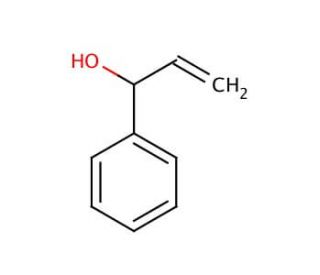
α-Vinylbenzyl alcohol (CAS 42273-76-7)
ACCÈS RAPIDE AUX LIENS
L'alcool α-vinylbenzyle (AVBA) est un composé chimique remarquable qui a suscité une grande attention dans la recherche scientifique, grâce à ses propriétés exceptionnelles et à ses diverses applications potentielles. Ce liquide incolore est soluble à la fois dans l'eau et dans les solvants organiques, ce qui le rend très polyvalent. L'une de ses principales utilisations réside dans la synthèse de divers polymères et copolymères. Des études approfondies ont été menées sur l'alcool α-vinylbenzyle afin d'explorer ses applications très variées dans de multiples domaines. Il sert de monomère précieux pour synthétiser divers polymères et copolymères. En copolymérisant l'alcool α-vinylbenzyle avec d'autres monomères comme le styrène, les acrylates et les méthacrylates, il est possible de produire des copolymères uniques aux propriétés distinctes. L'alcool α-vinylbenzyle présente une réactivité et peut subir diverses réactions chimiques, notamment la polymérisation, la réticulation et l'oxydation. Le mécanisme d'action de l'alcool α-vinylbenzyle dépend de son application spécifique. Dans la synthèse des polymères, il agit comme un monomère, subissant facilement des réactions de polymérisation pour donner des polymères et des copolymères.
α-Vinylbenzyl alcohol (CAS 42273-76-7) Références
- Réactions de type aldol et mannich via la migration in situ d'oléfines dans un liquide ionique. | Yang, XF., et al. 2003. Org Lett. 5: 657-60. PMID: 12605483
- Isomérisation redox très efficace d'alcools allyliques à température ambiante catalysée par de nouveaux complexes ruthénium-cyclopentadiényle: nouvelles perspectives sur le mécanisme. | Martín-Matute, B., et al. 2005. Chemistry. 11: 5832-42. PMID: 16028298
- Allylation très efficace et régiosélective avec des alcools allyliques catalysée par des grappes [Mo(3)S(4)Pd(eta(3)-allyl)]. | Tao, Y., et al. 2010. Org Lett. 12: 2726-9. PMID: 20469923
- Synthèse d'éthers de cinnamyle à partir d'alcool α-vinylbenzyle en utilisant l'iode comme catalyseur. | Kasashima, Y., et al. 2010. J Oleo Sci. 59: 549-55. PMID: 20877148
- Synthèse améliorée de Larock des quinolines via une réaction de Heck de 2-bromoanilines et d'alcools allyliques. | Stone, MT. 2011. Org Lett. 13: 2326-9. PMID: 21469650
- Synthèse chimio-enzymatique en milieu aqueux: combinaison de l'isomérisation de l'alcool allylique catalysée par un métal et de la bioamination asymétrique. | Ríos-Lombardía, N., et al. 2015. Chem Commun (Camb). 51: 10937-40. PMID: 26062926
- Amination allylique catalysée par le fer directement à partir d'alcools allyliques. | Emayavaramban, B., et al. 2016. Chemistry. 22: 3952-5. PMID: 26812622
- Allylation sélective en C-8 de la quinoléine: Une étude de cas de l'élimination β-Hydride vs β-Hydroxy. | Kalsi, D., et al. 2016. Org Lett. 18: 4198-201. PMID: 27533734
- Carboxylation efficace, régio- et stéréosélective, catalysée par le Pd, d'alcools allyliques avec de l'acide formique. | Fu, MC., et al. 2017. Chemistry. 23: 8818-8822. PMID: 28543768
- Guidage d'une réaction divergente par contrôle photochimique: accès sélectif bichromatique aux lévulinates et aux buténolides. | Sutar, RL., et al. 2018. Chem Sci. 9: 1368-1374. PMID: 29675185
- Isomérisation-méthylénation en tandem d'alcools allyliques à l'aide de palladium: synthèse monopot de 1,5-dikétones. | Samser, S., et al. 2021. J Org Chem. 86: 13744-13753. PMID: 34546055
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
α-Vinylbenzyl alcohol, 1 g | sc-233787 | 1 g | $61.00 |
