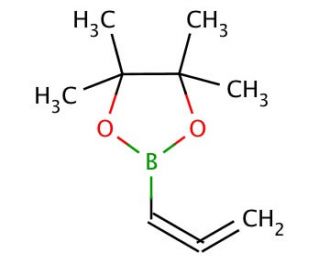
Allenylboronic acid pinacol ester (CAS 865350-17-0)
ACCÈS RAPIDE AUX LIENS
L'ester pinacol de l'acide allénylboronique est un composé polyvalent largement utilisé en synthèse organique et en recherche chimique pour sa capacité à participer à des réactions de couplage croisé, servant de précurseur pour la synthèse de structures moléculaires complexes. Ce composé est particulièrement apprécié pour son rôle dans les réactions de couplage de Suzuki-Miyaura, où il agit comme un réactif organoboron pour former des liaisons carbone-carbone avec des halogénures d'aryle ou de vinyle sous catalyse au palladium. La présence du groupe allényle dans la molécule permet la formation de systèmes hautement conjugués par des transformations ultérieures, ce qui permet aux chercheurs de construire des molécules architecturalement complexes avec précision. La partie pinacol ester de sa structure améliore sa stabilité et sa solubilité, ce qui facilite sa manipulation et son application dans diverses conditions de réaction. Son utilisation dans la synthèse chimique est essentielle pour le développement de nouveaux matériaux, catalyseurs et voies de synthèse, ce qui témoigne de son importance pour l'avancement du domaine de la chimie organique.
Allenylboronic acid pinacol ester (CAS 865350-17-0) Références
- Réactions d'annulation catalysées par le palladium pour la synthèse diastéréosélective du cyclopentène. | Kohn, BL. and Jarvo, ER. 2011. Org Lett. 13: 4858-61. PMID: 21854011
- Formation site- et énantiosélective de centres stéréogènes de carbone tertiaire ou quaternaire contenant de l'allène par substitution allylique catalysée par le NHC-Cu. | Jung, B. and Hoveyda, AH. 2012. J Am Chem Soc. 134: 1490-3. PMID: 22214185
- Comprendre le mécanisme de la propargylation asymétrique des aldéhydes promue par des catalyseurs dérivés du 1,1'-bi-2-naphtol. | Grayson, MN. and Goodman, JM. 2013. J Am Chem Soc. 135: 6142-8. PMID: 23517191
- Réactions de propargylation énantiosélective de N-Sulfonylkétimines catalysées par l'argent. | Osborne, CA., et al. 2015. Org Lett. 17: 5340-3. PMID: 26506430
- Seize cadres métal-organiques phosphonates isostructuraux avec une acidité de Lewis et une stabilité chimique contrôlées pour la catalyse asymétrique. | Chen, X., et al. 2017. Nat Commun. 8: 2171. PMID: 29259195
- Addition énantiosélective d'allényl-conjugué catalysée par le carbène N-hétérocyclique-Cu. | Chong, Q., et al. 2018. Org Lett. 20: 6896-6900. PMID: 30350670
- Méthode efficace de propargylation d'aldéhydes promue par des composés d'allénylboron sous irradiation micro-ondes. | Freitas, JJR., et al. 2020. Beilstein J Org Chem. 16: 168-174. PMID: 32117473
- Ester pinacol de l'acide allénylboronique: Un partenaire sélectif pour les cycloadditions [4 + 2]. | Labadie, N., et al. 2021. Org Lett. 23: 5081-5085. PMID: 34151574
- Réactivité Diels-Alder de l'ester pinacol de l'acide allénylboronique et des diénophiles apparentés: Études mécanistiques et analyse du modèle de déformation/interaction-activation. | Labadie, N. and Pellegrinet, SC. 2022. J Org Chem. 87: 16776-16784. PMID: 36440689
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Allenylboronic acid pinacol ester, 1 g | sc-262980 | 1 g | $153.00 | |||
Allenylboronic acid pinacol ester, 5 g | sc-262980A | 5 g | $520.00 |
