Alamethicin F50 (CAS 56165-93-6)
ACCÈS RAPIDE AUX LIENS
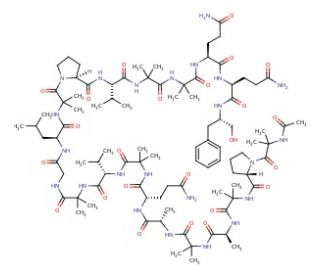
L'alaméthicine F50, identifiée par le numéro CAS 56165-93-6, est un antibiotique peptidique qui fait partie d'une classe plus large de composés connus sous le nom de peptaïbols, qui sont généralement produits par des champignons du genre Trichoderma. L'alaméthicine F50 est particulièrement remarquable pour son rôle dans la formation de canaux ioniques voltage-dépendants dans les bicouches phospholipidiques. Ce mécanisme implique l'insertion de la molécule d'alaméthicine dans une membrane lipidique, facilitée par sa nature amphipathique - elle possède à la fois des régions hydrophobes et hydrophiles. Une fois insérée, l'alaméthicine s'agrège pour former un faisceau hélicoïdal qui traverse la bicouche lipidique, créant ainsi un pore qui perturbe les gradients ioniques cellulaires. Cette perturbation permet un flux incontrôlé d'ions, en particulier de calcium et de sodium, à travers la membrane cellulaire, ce qui peut entraîner une augmentation de la perméabilité de la membrane et, en fin de compte, un dysfonctionnement cellulaire. En recherche, l'alaméthicine F50 a été largement utilisée pour étudier la biophysique membranaire, y compris la dynamique des interactions peptide-lipide et la modélisation fonctionnelle du comportement des canaux ioniques. Ces études sont cruciales pour comprendre les propriétés fondamentales des membranes cellulaires et le fonctionnement des canaux ioniques. Elles permettent de mieux comprendre les principes de base de l'électrophysiologie et les applications potentielles dans le développement de canaux ioniques synthétiques et de nouvelles méthodes de contrôle des processus bioélectriques dans les cellules.
Alamethicin F50 (CAS 56165-93-6) Références
- Activité des canaux ioniques des longibrachines LGA I et LGB II: effets des substitutions pro-2/Ala et gln-18/Glu sur les canaux membranaires voltage-gated de l'alaméthicine. | Cosette, P., et al. 1999. Biochim Biophys Acta. 1461: 113-22. PMID: 10556493
- Des conjugués de fullerènes et de lipopeptides d'alaméthicine auto-assemblés sans modèle forment des canaux ioniques voltage-dépendants d'une stabilité et d'une activité remarquables. | Jung, G., et al. 2003. J Pept Sci. 9: 784-98. PMID: 14658798
- Études sur la scission trifluoroacétolytique sélective de peptaïbols natifs et de peptides modèles à l'aide de la CLHP et de l'ESI-CID-MS. | Theis, C., et al. 2008. Chem Biodivers. 5: 2337-55. PMID: 19035563
- Biosynthèse de peptaïbols fluorés à l'aide d'une approche d'incorporation de blocs de construction dirigée par le site. | Rivera-Chávez, J., et al. 2017. J Nat Prod. 80: 1883-1892. PMID: 28594169
- Préalaméthicine F50 et peptaïbols apparentés de Trichoderma arundinaceum: Validation de leur authenticité par analyse chimique in situ. | Rivera-Chávez, J., et al. 2017. RSC Adv. 7: 45733-45751. PMID: 29379602
- La mélittine et une trichotoxine modifiée chimiquement forment des pores multiétatiques de type alaméthicine. | Hanke, W., et al. 1983. Biochim Biophys Acta. 727: 108-14. PMID: 6824646
- Effets des polycations sur les canaux ioniques formés par des alaméthicines neutres et chargées négativement. | Rink, T., et al. 1994. Eur Biophys J. 23: 155-65. PMID: 7525266
- La proline en position 14 de l'alaméthicine est essentielle pour l'activité hémolytique, la sécrétion de catécholamines par les cellules chromaffines et l'augmentation de l'activité métabolique dans les cellules endothéliales. | Dathe, M., et al. 1998. Biochim Biophys Acta. 1370: 175-83. PMID: 9518597
- Perméabilisation de la membrane et activité antimycoplasmique des peptaïbols à 18 résidus, les trichorzines PA. | Béven, L., et al. 1998. Biochim Biophys Acta. 1372: 78-90. PMID: 9651487
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Alamethicin F50, 2.5 mg | sc-391715 | 2.5 mg | $260.00 |
