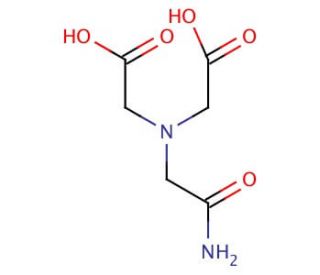
ADA (CAS 26239-55-4)
Voir les citations produits (1)
ACCÈS RAPIDE AUX LIENS
L'ADA, ou adénosine désaminase, est une enzyme largement étudiée en recherche biochimique pour son rôle critique dans le métabolisme des purines, où elle catalyse la désamination irréversible de l'adénosine en inosine. Dans les applications de recherche, l'ADA joue un rôle essentiel dans l'étude des voies métaboliques associées aux acides nucléiques et au transfert d'énergie. Les scientifiques utilisent cette enzyme pour étudier le métabolisme cellulaire et les mécanismes de régulation qui maintiennent l'équilibre des nucléotides dans les cellules, ce qui est essentiel pour le bon fonctionnement et la survie des cellules. L'activité de l'ADA est également utilisée en enzymologie pour comprendre la cinétique des réactions catalysées par les enzymes, ce qui permet de mieux comprendre le mécanisme, la spécificité et l'inhibition des enzymes. Cela a des implications plus larges dans le domaine de la biochimie, en particulier pour comprendre comment les altérations de l'activité enzymatique affectent les troubles métaboliques. Dans le domaine de la biotechnologie, l'ADA est utilisé dans la synthèse d'analogues de nucléosides, qui sont utiles comme outils biochimiques dans les expériences de biologie moléculaire et comme composés principaux potentiels dans la découverte de médicaments pour les maladies liées au dérèglement du métabolisme des purines. Grâce à son application dans ces domaines, l'ADA offre une fenêtre profonde sur les fonctions cellulaires et enzymatiques, améliorant notre compréhension des processus biologiques fondamentaux dans un contexte purement axé sur la recherche.
ADA (CAS 26239-55-4) Références
- Gradients de pH immobilisés: effet des sels, des ampholytes porteurs ajoutés et des gradients de tension sur les profils de protéines. | Righetti, PG., et al. 1988. Electrophoresis. 9: 65-73. PMID: 3234339
- Le tétramère d'histone H3-H4 est une enzyme réductrice de cuivre. | Attar, N., et al. 2020. Science. 369: 59-64. PMID: 32631887
- Structure cristalline de la protéine E2 du virus de la vaccine et perspectives sur la prédiction de nouveaux plis de protéines virales. | Gao, WND., et al. 2022. J Gen Virol. 103: PMID: 35020582
- Effets de l'huile essentielle de menthe poivrée sur les capacités d'apprentissage et de mémoire chez les souris transgéniques APP/PS1. | Lv, X., et al. 2022. Molecules. 27: PMID: 35408451
- Structure cristalline de la protéine de défense du phage BREX BrxA. | Beck, IN., et al. 2022. Curr Res Struct Biol. 4: 211-219. PMID: 35783086
- Étude thermodynamique, théorique et biologique combinée pour l'étude de l'acide N-(2-acétamido)iminodiacétique en tant qu'agent potentiel de décorporation du thorium. | Sharma, S., et al. 2023. Inorg Chem. 62: 18887-18900. PMID: 37922372
- Métabolomique assistée par une analyse transcriptomique pour révéler les caractéristiques métaboliques et les biomarqueurs potentiels associés à la réponse au traitement néoadjuvant avec le régime TCbHP dans le cancer du sein HER2 +. | Zhang, N., et al. 2024. Breast Cancer Res. 26: 64. PMID: 38610016
- Le rôle de la leucine 126 de l'histone H3 dans le réglage fin de l'activité cuivre-réductase des nucléosomes. | Tod, NP., et al. 2024. J Biol Chem. 300: 107314. PMID: 38657861
- Appauvrissement des ions métalliques libres par les tampons 'Good'. III. Complexes 2:1 de l'acide N-(2-acétamido)iminodiacétique avec le zinc(II), le cobalt(II), le nickel(II) et le cuivre(II); déprotonation de l'amide par le Zn(II), le Co(II) et le Cu(II). | Lance, EA., et al. 1983. Anal Biochem. 133: 492-501. PMID: 6314846
- Identification des isoformes de métallothionéine par électrophorèse de zone capillaire à l'aide d'un tube recouvert de polyacrylamide. | Minami, T., et al. 1996. J Chromatogr B Biomed Appl. 685: 353-9. PMID: 8953179
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
ADA, 25 g | sc-254936 | 25 g | $51.00 | |||
ADA, 100 g | sc-254936A | 100 g | $117.00 |
