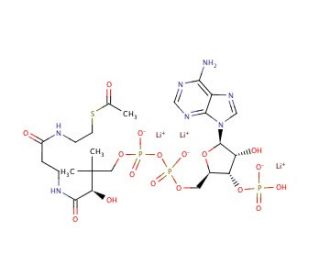
Structure moléculaire de Acetyl coenzyme A trilithium salt, Numéro CAS: 32140-51-5
Acetyl coenzyme A trilithium salt (CAS 32140-51-5)
Voir les citations produits (1)
Noms alternatifs:
Acetyl coenzyme A trilithium salt also known as Acetyl-S-CoA Li3; salt
Application(s):
Acetyl coenzyme A trilithium salt est un cofacteur et un transporteur de groupes acyles dans les réactions enzymatiques de transfert d'acétyle.
Numéro CAS:
32140-51-5
Masse Moléculaire:
881
Formule Moléculaire:
C23H35N7O17P3S•3Li
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Références bibliographiques
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le sel trilithium de l'acétyl coenzyme A est un sel de lithium d'un cofacteur essentiel et porteur de groupes acyles dans les réactions enzymatiques de transfert d'acétyle. Il est formé soit par la décarboxylation oxydative du pyruvate dans les mitochondries, soit par l'oxydation des acides gras à longue chaîne, soit par la dégradation oxydative de certains acides aminés. Le sel trilithium de l'acétyle-coenzyme A est un précurseur clé de la biosynthèse des lipides et la source de tous les carbones des acides gras. L'Acétyle est un régulateur positif de la pyruvate carboxylase et un précurseur du neurotransmetteur acétylcholine.
Acetyl coenzyme A trilithium salt (CAS 32140-51-5) Références
- Les inhibiteurs de l'oxyde nitrique synthase atténuent les augmentations de l'expression de la choline acétyltransférase médiées par le facteur de croissance nerveuse dans les cellules PC12. | Kalisch, BE., et al. 2002. J Neurochem. 81: 624-35. PMID: 12065671
- Enzymes du métabolisme du poly-(bêta)-hydroxybutyrate dans les bactéroïdes du soja et du pois chiche. | Kim, SA. and Copeland, L. 1996. Appl Environ Microbiol. 62: 4186-90. PMID: 16535445
- Modifications des histones induites par le formaldéhyde in vitro. | Lu, K., et al. 2008. Chem Res Toxicol. 21: 1586-93. PMID: 18656964
- Bioconjugués enzyme-nanoparticule avec deux enzymes séquentielles: stœchiométrie et activité de la malate déshydrogénase et de la citrate synthase sur des nanoparticules d'Au. | Keighron, JD. and Keating, CD. 2010. Langmuir. 26: 18992-9000. PMID: 21114258
- Méthodes d'analyse de l'acétyl-CoA synthase: applications aux systèmes bactériens et archéologiques. | Grahame, DA. 2011. Methods Enzymol. 494: 189-217. PMID: 21402216
- Analyse LC-MS/MS du coenzyme A et des acyl-coenzyme A thioesters à chaîne courte. | Neubauer, S., et al. 2015. Anal Bioanal Chem. 407: 6681-8. PMID: 26168961
- La sonde mitochondriale Methyltriphenylphosphonium (TPMP) inhibe l'enzyme du cycle de Krebs 2-Oxoglutarate Dehydrogenase. | Elkalaf, M., et al. 2016. PLoS One. 11: e0161413. PMID: 27537184
- Cinétique de la génération d'électrons intracellulaires chez Shewanella oneidensis MR-1. | Ishiki, K. and Shiigi, H. 2019. Anal Chem. 91: 14401-14406. PMID: 31631651
- Acétylation N-Terminal in vitro de parvalbumines exprimées bactériennement par des acétyltransférases N-Terminal d'Escherichia coli. | Lapteva, YS., et al. 2021. Appl Biochem Biotechnol. 193: 1365-1378. PMID: 32394317
- N-acétyltransférases hépatiques: inactivation sélective in vivo par un acide N-arylhydroxamique cancérigène. | Smith, TJ. and Hanna, PE. 1988. Biochem Pharmacol. 37: 427-34. PMID: 3257389
- Changements dans les isoenzymes de la malate déshydrogénase au cours de la différenciation des cellules érythroïdes de la moelle osseuse de lapin. | Setchenska, MS. and Arnstein, HR. 1979. Int J Biochem. 10: 817-21. PMID: 510663
- Prévention des défauts de transport axonal et de vitesse de conduction nerveuse par l'administration orale de myo-inositol ou d'un inhibiteur de l'aldose réductase chez des rats diabétiques à la streptozotocine. | Mayer, JH. and Tomlinson, DR. 1983. Diabetologia. 25: 433-8. PMID: 6197336
- Toxicité développementale et métabolisme comparés du nitrazépam chez le rat et la souris. | Takeno, S., et al. 1993. Toxicol Appl Pharmacol. 121: 233-8. PMID: 8346540
- Rôle clé de l'acétyl-CoA dans le cytoplasme des terminaisons nerveuses dans les perturbations du métabolisme de l'acétylcholine dans le cerveau. | Szutowicz, A., et al. 1997. Folia Neuropathol. 35: 241-3. PMID: 9833402
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Acetyl coenzyme A trilithium salt, 1 mg | sc-214465 | 1 mg | $69.00 | |||
Acetyl coenzyme A trilithium salt, 5 mg | sc-214465A | 5 mg | $119.00 | |||
Acetyl coenzyme A trilithium salt, 25 mg | sc-214465B | 25 mg | $389.00 | |||
Acetyl coenzyme A trilithium salt, 100 mg | sc-214465C | 100 mg | $1099.00 | |||
Acetyl coenzyme A trilithium salt, 250 mg | sc-214465D | 250 mg | $2599.00 | |||
Acetyl coenzyme A trilithium salt, 1 g | sc-214465E | 1 g | $6863.00 |
