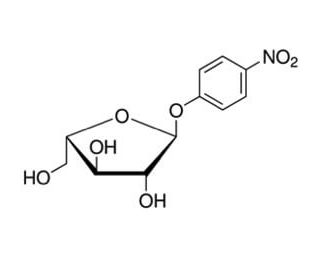
Structure moléculaire de 4-Nitrophenyl α-L-arabinofuranoside, Numéro CAS: 6892-58-6
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6)
Voir les citations produits (1)
Noms alternatifs:
pNP-alpha-L-Arabinofuranoside
Numéro CAS:
6892-58-6
Pureté:
≥98%
Masse Moléculaire:
271.22
Formule Moléculaire:
C11H13NO7
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Références bibliographiques
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le 4-nitrophényl α-L-arabinofuranoside est un composé synthétique souvent utilisé en biochimie et en biologie moléculaire comme substrat chromogène dans le dosage de l'activité de l'α-L-arabinofuranosidase. Les α-L-Arabinofuranosidases sont des enzymes qui catalysent l'hydrolyse des liaisons α-L-arabinofuranosides, que l'on trouve dans divers composés naturels, y compris les polysaccharides et les glycoconjugués. Ces enzymes jouent un rôle dans la décomposition et le métabolisme des glucides complexes, contribuant à la dégradation de la biomasse végétale et au cycle de la matière organique dans l'environnement.
4-Nitrophenyl α-L-arabinofuranoside (CAS 6892-58-6) Références
- Glycoside hydrolases bifonctionnelles de la famille 3 de l'orge avec activité alpha -L-arabinofuranosidase et bêta -D-xylosidase. Caractérisation, structures primaires et traitement COOH-terminal. | Lee, RC., et al. 2003. J Biol Chem. 278: 5377-87. PMID: 12464603
- Les acétates de p-nitrophényl alpha-L-arabinofuranoside - préparation régiosélective par l'action des lipases. | Mastihubová, M., et al. 2006. Bioorg Med Chem. 14: 1805-10. PMID: 16288881
- Variation de la spécificité relative du substrat de la bêta-D-xylosidase/alpha-L-arabinofuranosidase bifonctionnelle par des mutations à site unique: rôles de la distorsion et de la reconnaissance du substrat. | Jordan, DB. and Li, XL. 2007. Biochim Biophys Acta. 1774: 1192-8. PMID: 17689155
- Construction et caractérisation de deux enzymes chimériques dégradant le xylane. | Fan, Z., et al. 2009. Biotechnol Bioeng. 102: 684-92. PMID: 18828173
- Thermodynamique des réactions d'hydrolyse de l'acétate de 1-naphtyle, de l'acétate de 4-nitrophényle et de l'α-L-arabinofuranoside de 4-nitrophényle. | Decker, SR., et al. 2010. J Phys Chem B. 114: 16060-7. PMID: 20361764
- Nouvelle alpha-L-arabinofuranosidase/xylobiohydrolase bifonctionnelle (ABF3) de Penicillium purpurogenum. | Ravanal, MC., et al. 2010. Appl Environ Microbiol. 76: 5247-53. PMID: 20562284
- Action des enzymes de désacétylation du xylane sur les dérivés monoacétyles des glycosides 4-nitrophényl de β-D-xylopyranose et α-L-arabinofuranose. | Biely, P., et al. 2011. J Biotechnol. 151: 137-42. PMID: 21029756
- Purification et caractérisation de l'arabinofuranosidase de l'endophyte du maïs Acremonium zeae. | Bischoff, KM., et al. 2011. Biotechnol Lett. 33: 2013-8. PMID: 21671092
- L'analyse de la famille de gènes de l'arabinoxylane arabinofuranohydrolase chez l'orge ne confirme pas leur implication dans le remodelage des parois cellulaires de l'endosperme au cours du développement. | Laidlaw, HK., et al. 2012. J Exp Bot. 63: 3031-45. PMID: 22378943
- Activation d'une β-xylosidase GH43 par un métal divalent. | Lee, CC., et al. 2013. Enzyme Microb Technol. 52: 84-90. PMID: 23273276
- Une nouvelle exo-α-l-arabinofuranosidase/endo-xylanase GH51 bifonctionnelle d'Alicyclobacillus sp. A4 avec une capacité significative de dégradation de la biomasse. | Yang, W., et al. 2015. Biotechnol Biofuels. 8: 197. PMID: 26628911
- Caractérisation d'une arabinofuranosidase putative de la famille des glycosides hydrolases 43 d'Aspergillus niger et son utilisation potentielle dans la production de bière. | Li, X., et al. 2020. Food Chem. 305: 125382. PMID: 31525590
- Caractérisation et analyse fonctionnelle de deux nouvelles α-L-arabinofuranosidases thermotolérantes appartenant à la famille des glycosides hydrolases 51 de Thielavia terrestris et à la famille 62 d'Eupenicillium parvum. | Long, L., et al. 2020. Appl Microbiol Biotechnol. 104: 8719-8733. PMID: 32880690
- La bêta-D-xylosidase de Trichoderma reesei est une bêta-D-xylane xylohydrolase multifonctionnelle. | Herrmann, MC., et al. 1997. Biochem J. 321 (Pt 2): 375-81. PMID: 9020869
- Purification et caractérisation d'une nouvelle alpha-L-arabinofuranosidase thermostable provenant d'une souche colorée d'Aureobasidium pullulans. | Saha, BC. and Bothast, RJ. 1998. Appl Environ Microbiol. 64: 216-20. PMID: 9435077
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
4-Nitrophenyl α-L-arabinofuranoside, 10 mg | sc-220982 | 10 mg | $109.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 25 mg | sc-220982A | 25 mg | $203.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 50 mg | sc-220982B | 50 mg | $359.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 100 mg | sc-220982C | 100 mg | $515.00 | |||
4-Nitrophenyl α-L-arabinofuranoside, 250 mg | sc-220982D | 250 mg | $983.00 |
