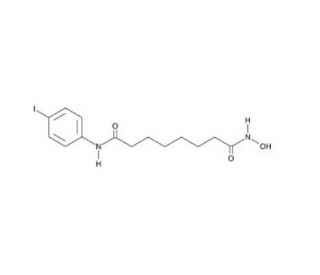
4-iodo-SAHA (CAS 1219807-87-0)
ACCÈS RAPIDE AUX LIENS
Le 4-iodo-SAHA, appelé 4-iodo-N-hydroxyoctanediamide (IHOD), est un composé organique synthétique. Ce solide incolore est soluble dans divers solvants, notamment l'eau, l'éthanol et le sulfoxyde de diméthyle. Le 4-iodo-SAHA est un réactif polyvalent dans la synthèse chimique, un catalyseur dans les réactions biochimiques et un ligand dans les études de liaison aux protéines. Dans les réactions biochimiques, le 4-iodo-SAHA joue le rôle de catalyseur. Il se lie au substrat, permettant sa conversion en produit. La présence de 4-iodo-SAHA facilite la réaction en interagissant avec l'enzyme, améliorant ainsi son efficacité. En outre, le 4-iodo-SAHA agit comme un ligand dans les études de liaison aux protéines, où il se lie à la protéine cible, contribuant ainsi à la stabilisation de sa structure. En résumé, le 4-iodo-SAHA, ou 4-iodo-N-hydroxyoctanediamide (IHOD), est un composé organique synthétique largement utilisé dans la recherche scientifique. Sa polyvalence en tant que réactif, catalyseur et ligand lui permet d'être utilisé dans diverses applications de recherche.
4-iodo-SAHA (CAS 1219807-87-0) Références
- Des dérivés d'inhibiteurs d'histone désacétylase de l'acide suberoylanilide hydroxamique à groupe cap modifié révèlent une activité antileucémique sélective améliorée. | Salmi-Smail, C., et al. 2010. J Med Chem. 53: 3038-47. PMID: 20218673
- Le criblage des inhibiteurs de l'histone désacétylase identifie la toxine HC comme la plus efficace dans les cellules de cholangiocarcinome intrahépatique. | Zhou, W., et al. 2016. Oncol Rep. 35: 2535-42. PMID: 26935789
- Un criblage de médicaments basé sur l'imagerie identifie les inhibiteurs d'HDAC comme de nouveaux perturbateurs de Golgi synergiques avec JQ1. | Gendarme, M., et al. 2017. Mol Biol Cell. 28: 3756-3772. PMID: 29074567
- Ingénierie de la capacité de lignage et de la plasticité des cellules souches à l'aide de molécules épigénétiques. | Dhaliwal, A., et al. 2018. Sci Rep. 8: 16289. PMID: 30389989
- Développement d'un essai de criblage à haut débit basé sur les cellules pour identifier les composés induisant des peptides de défense de l'hôte porcin. | Deng, Z., et al. 2018. J Immunol Res. 2018: 5492941. PMID: 30581875
- L'inhibiteur d'histone désacétylase Suberoylanilide Hydroxamic Acid supprime l'expression génétique et la réplication de l'adénovirus humain. | Saha, B. and Parks, RJ. 2019. J Virol. 93: PMID: 30944181
- Les inhibiteurs épigénétiques ciblent plusieurs stades du parasite Plasmodium falciparum. | Coetzee, N., et al. 2020. Sci Rep. 10: 2355. PMID: 32047203
- Le criblage d'une bibliothèque de médicaments épigénétiques identifie le 4-((hydroxyamino)carbonyl)-N-(2-hydroxyethyl)-N-Phenyl-Benzeneacetamide qui réduit la synthèse de la mélanine en inhibant l'activité de la tyrosinase indépendamment des mécanismes épigénétiques. | Song, H., et al. 2020. Int J Mol Sci. 21: PMID: 32605171
- Liaison des inhibiteurs aux mutants du site actif de CD1, l'énigmatique domaine catalytique de l'histone désacétylase 6. | Osko, JD. and Christianson, DW. 2020. Acta Crystallogr F Struct Biol Commun. 76: 428-437. PMID: 32880591
- Identification d'inhibiteurs de la réplication de l'adénovirus humain à partir d'une bibliothèque de petites molécules ciblant les régulateurs épigénétiques cellulaires. | Saha, B. and Parks, RJ. 2021. Virology. 555: 102-110. PMID: 33032802
- Un nouvel écran de combinaisons chimiques chez le poisson zèbre identifie des petites molécules épigénétiques candidates pour le traitement de la dystrophie musculaire de Duchenne. | Farr, GH., et al. 2020. Skelet Muscle. 10: 29. PMID: 33059738
- Des inhibiteurs d'histone désacétylase sélectionnés inversent le défaut transcriptionnel de la Frataxine dans un nouveau système rapporteur neuronal dérivé de cellules souches pluripotentes induites par l'ataxie de Friedreich. | Schreiber, AM., et al. 2022. Front Neurosci. 16: 836476. PMID: 35281493
- Amélioration de la chromatine et de la reprogrammation épigénétique dans les embryons porcins SCNT - Progrès et perspectives. | Glanzner, WG., et al. 2022. Front Cell Dev Biol. 10: 940197. PMID: 35898400
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
4-iodo-SAHA, 50 mg | sc-364391 | 50 mg | $150.00 | |||
4-iodo-SAHA, 250 mg | sc-364391A | 250 mg | $676.00 |
