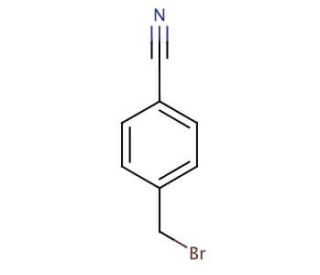
4-Cyanobenzyl Bromide (CAS 17201-43-3)
ACCÈS RAPIDE AUX LIENS
Le bromure de 4-cyanobenzyle est un halogénure de benzyle utilisé comme herbicide de post-levée. Le bromure de 4-cyanobenzyle (4-CBB) a acquis une grande popularité dans la recherche scientifique en raison de sa remarquable polyvalence et de ses diverses applications dans la synthèse de divers composés. Agissant à la fois comme réactif et comme catalyseur dans la synthèse organique, il joue un rôle dans la création de produits pharmaceutiques et d'autres composés bioactifs. En outre, il sert d'intermédiaire précieux dans ces processus de synthèse. Son utilité va plus loin puisqu'il sert de système modèle pour explorer la cinétique et les mécanismes des réactions organiques. Le bromure de 4-cyanobenzyle est très utilisé dans la recherche scientifique. Il sert de réactif dans la synthèse organique, de catalyseur dans les réactions organiques et d'intermédiaire essentiel dans la production de produits pharmaceutiques et de composés bioactifs. En outre, les chercheurs l'utilisent comme un modèle précieux pour étudier la cinétique et les mécanismes complexes des réactions organiques. Ses applications sont encore plus variées, englobant la synthèse de peptides, de peptidomimétiques et de nucléosides. Le mécanisme d'action du bromure de 4-cyanobenzyle repose sur sa capacité à interagir avec divers groupes fonctionnels. Ses réactions avec les aldéhydes, les cétones et les acides carboxyliques produisent des esters, tandis qu'il forme des amides avec les amines. En outre, le bromure de 4-cyanobenzyle peut créer des éthers lorsqu'il réagit avec des alcools et des thioéthers lorsqu'il réagit avec des thiols. Ces réactions polyvalentes le rendent utile aux scientifiques qui explorent les subtilités de la chimie organique.
4-Cyanobenzyl Bromide (CAS 17201-43-3) Références
- Aminoborohydrides. 12. Nouvelles réactions tandem d'amination-réduction S(N)Ar de 2-halobenzonitriles avec des N,N-dialkylaminoborohydrides de lithium. | Thomas, S., et al. 2001. J Org Chem. 66: 1999-2004. PMID: 11300892
- Stabilité des adduits ioniques/radicalaires en phase liquide, dérivée de la dépendance des réactivités de clivage électrochimique par rapport au solvant. | Pause, L., et al. 2001. J Am Chem Soc. 123: 11908-16. PMID: 11724597
- Activité trypanocide de congénères de pentamidine conformationnellement restreints. | Donkor, IO., et al. 2003. J Med Chem. 46: 1041-8. PMID: 12620080
- Inhibiteurs aryl-tétrahydropyridiniques de la farnésyltransférase: analogues biodisponibles avec une puissance cellulaire améliorée. | Gwaltney, SL., et al. 2003. Bioorg Med Chem Lett. 13: 1363-6. PMID: 12657283
- Conception, synthèse et évaluation biologique de nouveaux 2-pyridinyl-[1,2,4]triazoles en tant qu'inhibiteurs du récepteur de type 1 du facteur de croissance transformant bêta1. | Kim, DK., et al. 2004. Bioorg Med Chem. 12: 2013-20. PMID: 15080905
- Sondes basées sur l'activité pour les protéines tyrosine phosphatases. | Kumar, S., et al. 2004. Proc Natl Acad Sci U S A. 101: 7943-8. PMID: 15148367
- Réactions progressives et concertées de transfert d'électrons/rupture de liaisons. Contrôle par le solvant de l'existence de radicaux pi instables et des barrières d'activation de leur clivage hétérolytique. | Costentin, C., et al. 2004. J Am Chem Soc. 126: 16834-40. PMID: 15612722
- Synthèse et études PET du [(11)C-cyano]létrozole (Femara), un médicament inhibiteur de l'aromatase. | Kil, KE., et al. 2009. Nucl Med Biol. 36: 215-23. PMID: 19217534
- Nouveaux complexes N-heterocyclic carbene-silver acetate substitués par des benzyles: synthèse, cytotoxicité et études antibactériennes. | Patil, S., et al. 2011. Metallomics. 3: 74-88. PMID: 21135954
- Le groupe nitrile comme sonde infrarouge pour la caractérisation de la conformation de l'albumine sérique bovine solubilisée dans des micelles inversées. | Xue, L., et al. 2012. Spectrochim Acta A Mol Biomol Spectrosc. 97: 858-63. PMID: 22902928
- Un motif N-(acétoxy)phtalimide comme pro-photosensibilisateur de la lumière visible dans l'arylthiation décarboxale photoredox. | Jin, Y., et al. 2016. Chem Commun (Camb). 52: 12909-12912. PMID: 27739553
- Inversion stéréochimique des oscillations moléculaires du pilier[5]arène différencié par le bord. | Du, K., et al. 2020. J Org Chem. 85: 11368-11374. PMID: 32820630
- Synthèse et effets antiplaquettaires d'une série isoxazole d'antagonistes de la glycoprotéine IIb/IIIa. | Xue, CB., et al. 1998. Bioorg Med Chem Lett. 8: 3499-504. PMID: 9934460
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
4-Cyanobenzyl Bromide, 5 g | sc-216817 | 5 g | $23.00 |
