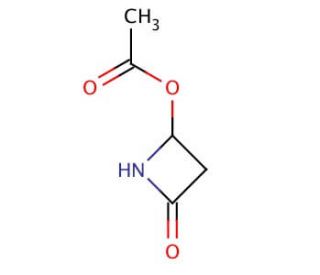
Structure moléculaire de 4-Acetoxy-2-azetidinone, Numéro CAS: 28562-53-0
4-Acetoxy-2-azetidinone (CAS 28562-53-0)
Numéro CAS:
28562-53-0
Masse Moléculaire:
129.11
Formule Moléculaire:
C5H7NO3
Information supplémentaire:
Ce produit est classé comme marchandise dangereuse pour le transport et peut faire l'objet de frais d'expédition supplémentaires.
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
La 4-acétoxy-2-azétidinone sert de modèle dans la synthèse des β-aminoacides. Un processus d'allylation en position α produit un énolate, qui peut ensuite réagir avec un nucléophile azoté pour produire un groupe carbonyle insaturé α,β. L'unité carbonyle polyvalente peut être soit hydrolysée pour produire un groupe hydroxyle, soit chlorée pour produire un chlorure. Il a été utilisé dans la synthèse asymétrique comme auxiliaire chiral. En outre, il joue un rôle dans la synthèse de cyclopentènes dérivés, présentant une grande régio- et diastéréosélectivité. Il a également été utilisé comme synthon hétérocyclique pour des agents antibiotiques et anti-inflammatoires.
4-Acetoxy-2-azetidinone (CAS 28562-53-0) Références
- L'introduction sélective de groupes allényles et propargyles en position C4 de 2-azétidinones, médiée par l'indium, et la cyclisation de 4-allényl-2-azétidinones catalysée par AuCl3. | Lee, PH., et al. 2005. Angew Chem Int Ed Engl. 44: 1840-3. PMID: 15714454
- 1,2,4,5-hexatétraen-3-ylation de 4-acétoxy-2-azétidinones médiée par l'indium et leurs applications aux réactions de Diels-Alder pour la synthèse de dérivés de 2-azétidinones. | Yu, H. and Lee, PH. 2008. J Org Chem. 73: 5183-6. PMID: 18507447
- Additions allyliques médiées par le Pd(0)/InI à la 4-acétoxy-2-azétidinone: nouvelle voie vers des échafaudages carbocycliques hautement fonctionnalisés. | Cesario, C. and Miller, MJ. 2009. Org Lett. 11: 1293-5. PMID: 19216521
- Synthèses d'analogues carbocycliques de l'uracile polyoxine C: application de l'alylation Pd(0)/InI de la 4-acétoxy-2-azétidinone. | Cesario, C. and Miller, MJ. 2009. J Org Chem. 74: 5730-3. PMID: 19514728
- Études phytochimiques, potentiel antioxydant et identification des composés bioactifs par GC-MS de l'extrait éthanolique du fruit de Luffa cylindrica (L.). | S, AS. and Vellapandian, C. 2022. Appl Biochem Biotechnol. 194: 4018-4032. PMID: 35583705
- Réaction de la 4-acétoxy-2-azétidinone avec des carbanions tertiaires: Préparation de 4-alkyl- et 4-alkylidène-2-azétidinones | C.W. Greengrass ∗, D.W.T. Hoople. 1981. Tetrahedron Letters. 22: 1161-1164.
- Etudes sur les 1-carbadethiacephems, partie II: Réaction de 4-acetoxy-2-azetidinone avec des énolates d'aluminium | C.W. Greengrass ∗, M.S. Nobbs. 1981. Tetrahedron Letters. 22: 5339-5340.
- Nouvelle synthèse de 4-acétoxy-2-azétidinones par oxydation électrochimique | Miwako Mori ∗, Katsuji Kagechika, Koh Tohjima, Masakatsu Shibasaki ∗. 1988. Tetrahedron Letters. 29: 1409-1412.
- 2-aza-1,3-diènes comme nouveaux précurseurs pour la synthèse de β-lactames non substitués. Synthèse en trois étapes de la 4-acétoxy-3-phénoxy-2-azéridinone | Gunda I Georg ∗, Joydeep Kant, Ping He, Ana Maria Ly, Lynn Lampe 1. 1988. Tetrahedron Letters. 29: 2409-2412.
- Réaction de la 2-azétidinone substituée en position 4 avec des nucléophiles. Existence et réactivité de la 1-azétine-4-one | Francisco Gavina, Ana M. Costero, and M. Rosario Andreu, et al. 1990. J. Org. Chem. 55: 434–437.
- Synthèse hautement stéréocontrôlée de l'intermédiaire clé 1β-méthylcarbapénème par la réaction de reformatsky de dérivés de 3-(2-bromopropionyl)-2-oxazolidone avec un 4-acétoxy-2-azétidinon | Yoshio Ito a 1, Akira Sasaki b, Kastumi Tamoto b, Makoto Sunagawa b, Shiro Terashima ∗ a. 1991. Tetrahedron. 47: 2801-2820.
- Synthèse de 4-allenyl et de 4-proparyl-2-azetidinone par réaction de type Barbier médiée par le Zn et amidation intramoléculaire catalysée par le Pt pour obtenir des squelettes de carbapénèmes | Biao Jiang, Hua Tian. 2007. Tetrahedron Letters. 48: 7942-7945.
- Approche synthétique pratique de la 4-acétoxy-2-azétidinone pour la préparation d'antibiotiques de type carbapénème et pénème | Guo-Bin Zhou, Yue-Qing Guan, He Tang, Yan-Bin Zhao & Li-Rong Yang. 2012. Research on Chemical Intermediates. 38: 251–259.
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
4-Acetoxy-2-azetidinone, 1 g | sc-254591 | 1 g | $92.00 |
