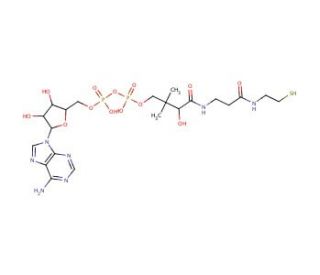
Structure moléculaire de 3'-Dephosphocoenzyme A, Numéro CAS: 3633-59-8
3′-Dephosphocoenzyme A (CAS 3633-59-8)
Noms alternatifs:
Dephospho CoA
Application(s):
3'-Dephosphocoenzyme A est un réactif chimique qui est le précurseur direct de la coenzyme A. Il est utilisé pour la synthèse de la coenzyme A par la CoA Synthase bifonctionnelle.
Numéro CAS:
3633-59-8
Pureté:
≥90%
Masse Moléculaire:
687.55
Formule Moléculaire:
C21H35N7O13P2S
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
Le 3'-déphosphocoenzyme A est un réactif chimique qui est le précurseur direct du coenzyme A. Il est utilisé pour la synthèse du coenzyme A par la CoA Synthase bifonctionnelle. Le 3'-déphosphocoenzyme A peut servir d'initiateur de transcription lors de la transcription in vitro pour la synthèse de l'ARN-CoA. Il appartient à la catégorie des ribonucléosides puriques diphosphates, qui sont des ribonucléotides puriques liés au ribose avec un groupe diphosphate. Il est donc considéré comme une molécule lipidique appartenant à la classe des esters gras.
3′-Dephosphocoenzyme A (CAS 3633-59-8) Références
- Valproyl-dephosphoCoA: un nouveau métabolite du valproate formé in vitro dans les mitochondries du foie de rat. | Silva, MF., et al. 2004. Drug Metab Dispos. 32: 1304-10. PMID: 15483197
- Ingénierie des voies métaboliques pour la biosynthèse de polykétides complexes chez Saccharomyces cerevisiae. | Mutka, SC., et al. 2006. FEMS Yeast Res. 6: 40-7. PMID: 16423069
- Nouvelles connaissances sur l'activation et la reconnaissance du substrat de la polyhydroxyalcanoate synthase de Ralstonia eutropha. | Ushimaru, K., et al. 2013. Appl Microbiol Biotechnol. 97: 1175-82. PMID: 22543354
- L'haploinsuffisance de Ranbp2 entraîne des phénotypes cellulaires et biochimiques distincts dans les cellules dopaminergiques et gliales du cerveau et de la rétine, provoqués par la neurotoxine parkinsonienne, le 1-méthyl-4-phényl-1,2,3,6-tétrahydropyridine (MPTP). | Cho, KI., et al. 2012. Cell Mol Life Sci. 69: 3511-27. PMID: 22821000
- Étude aux rayons X des changements de conformation de la molécule de phosphopantethéine adénylyltransférase de Mycobacterium tuberculosis au cours de la réaction catalysée. | Timofeev, V., et al. 2012. Acta Crystallogr D Biol Crystallogr. 68: 1660-70. PMID: 23151631
- Blocage sélectif du canal Kv1.3 comme traitement de l'obésité et de la résistance à l'insuline. | Upadhyay, SK., et al. 2013. Proc Natl Acad Sci U S A. 110: E2239-48. PMID: 23729813
- La transition de la phosphopantethéine adénylyltransférase de l'état catalytique à l'état allostérique est caractérisée par la formation d'un complexe ternaire chez Pseudomonas aeruginosa. | Chatterjee, R., et al. 2016. Biochim Biophys Acta. 1864: 773-86. PMID: 27041211
- Caractérisation et analyse quantitative des substances apparentées dans le coenzyme A par HPLC et LC-MS/MS. | Yang, Y., et al. 2018. J Pharm Biomed Anal. 150: 220-232. PMID: 29253778
- Détermination de la capacité bioénergétique d'oxydation des acides gras dans le système nerveux des mammifères. | White, CJ., et al. 2020. Mol Cell Biol. 40: PMID: 32123009
- Évaluation comparative des flux d'acquisition dépendants et indépendants des données mis en œuvre sur une fusion Orbitrap pour la métabolomique non ciblée. | Barbier Saint Hilaire, P., et al. 2020. Metabolites. 10: PMID: 32325648
- Métabolisme des protéines porteuses d'acyle et régulation de la biosynthèse des acides gras par Lactobacillus plantarum. | Sabaitis, JE. and Powell, GL. 1976. J Biol Chem. 251: 4706-12. PMID: 780354
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
3′-Dephosphocoenzyme A, 5 mg | sc-214187 | 5 mg | $239.00 | |||
3′-Dephosphocoenzyme A, 25 mg | sc-214187A | 25 mg | $819.00 |
