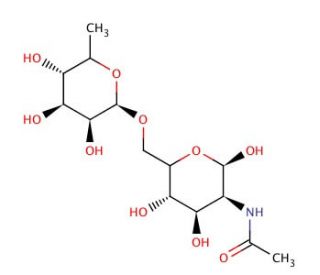
2-Acetamido-2-deoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose (CAS 33639-80-4)
ACCÈS RAPIDE AUX LIENS
Le 2-acétamido-2-désoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose est un composé qui joue un rôle crucial dans la biosynthèse des glycoprotéines et des glycolipides. Plus précisément, il sert de substrat aux enzymes glycosyltransférases impliquées dans l'attachement des résidus fucose aux chaînes glycanniques. Ce produit chimique est particulièrement important dans le contexte de la communication cellulaire et des processus de reconnaissance médiés par les glycoconjugués de la surface cellulaire. La recherche sur le 2-acétamido-2-désoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose se concentre sur l'élucidation des voies enzymatiques responsables de la fucosylation et de son rôle dans divers phénomènes biologiques, y compris la modulation de la réponse immunitaire, l'adhésion cellulaire et la signalisation. Des études ont identifié des glycosyltransférases spécifiques et des facteurs de régulation impliqués dans l'ajout de résidus fucose aux structures glycanniques, soulignant l'importance du 2-Acetamido-2-deoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose en tant que substrat dans ces réactions enzymatiques. En outre, ce composé est un outil précieux dans la recherche en glycobiologie pour étudier les relations structure-fonction des molécules de glycane et leur impact sur les processus cellulaires. En comprenant les mécanismes qui régissent la fucosylation et la biosynthèse des glycanes, les chercheurs visent à découvrir de nouvelles cibles d'intervention dans les maladies associées à des schémas de glycosylation aberrants, telles que le cancer, l'inflammation et les troubles auto-immuns. En outre, le 2-acétamido-2-désoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose est utilisé dans des stratégies de synthèse chimique pour produire des sondes glycanniques structurellement définies afin d'étudier les interactions glycanes-protéines et de développer des approches de glyco-ingénierie pour des applications biotechnologiques et biomédicales.
2-Acetamido-2-deoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose (CAS 33639-80-4) Références
- Base structurelle de l'interaction entre les oligosaccharides du lait humain et la lectine bactérienne PA-IIL de Pseudomonas aeruginosa. | Perret, S., et al. 2005. Biochem J. 389: 325-32. PMID: 15790314
- La lectine LecB de Pseudomonas aeruginosa est située dans la membrane externe et participe à la formation du biofilm. | Tielker, D., et al. 2005. Microbiology (Reading). 151: 1313-1323. PMID: 15870442
- Structures de rayons X et thermodynamique de l'interaction du PA-IIL de Pseudomonas aeruginosa avec des dérivés de disaccharides. | Marotte, K., et al. 2007. ChemMedChem. 2: 1328-38. PMID: 17623286
- Adaptation des loci d'utilisation du xyloglucane synténique des bactéroïdètes de l'intestin humain à la diversité des chaînes latérales des polysaccharides. | Déjean, G., et al. 2019. Appl Environ Microbiol. 85: PMID: 31420336
- Aperçu structurel de deux nouvelles enzymes N-acétyl-glucosaminidase grâce à des méthodes in silico. | ŞahutoĞlu, AS., et al. 2020. Turk J Chem. 44: 1703-1712. PMID: 33488263
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
2-Acetamido-2-deoxy-6-O-(α-L-fucopyranosyl)-D-glucopyranose, 2.5 mg | sc-220679 | 2.5 mg | $263.00 |
