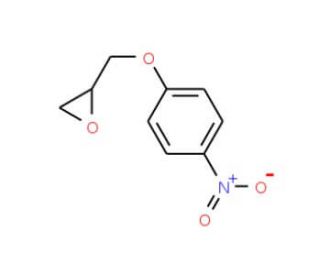
1,2-Epoxy-3-(4-nitrophenoxy)propane (CAS 5255-75-4)
Voir les citations produits (2)
ACCÈS RAPIDE AUX LIENS
Le 1,2-époxy-3-(4-nitrophénoxy)propane (ENPP) a attiré l'attention pour ses applications potentielles dans les domaines de la chimie organique synthétique et de la science des matériaux. Ce composé organique, doté d'un cycle éther cyclique à trois membres, sert d'intermédiaire dans la synthèse de divers composés organiques, notamment des polymères, des hétérocycles et des produits naturels. En outre, ses propriétés catalytiques ont facilité la synthèse de polymères et d'autres matériaux. En outre, le 1,2-époxy-3-(4-nitrophénoxy)propane est utilisé comme ligand pour la synthèse de complexes métalliques, comme réactif dans la synthèse de polymères et comme catalyseur pour la polymérisation de monomères. Bien que le mécanisme d'action précis du 1,2-Epoxy-3-(4-nitrophenoxy)propane reste flou, on suppose que la réaction implique l'attaque nucléophile du p-nitrophénol sur l'oxyde de propylène. Cette attaque est suivie par la formation d'une liaison éther entre les deux composants. On pense qu'un acide de Lewis, tel que le trifluorure de bore, sert de catalyseur pour cette réaction.
1,2-Epoxy-3-(4-nitrophenoxy)propane (CAS 5255-75-4) Références
- La détoxification des précurseurs de la chaîne latérale de la pénicilline dépend-elle de la monooxygénase microsomale et de la glutathion S-transférase chez Penicillium chrysogenum ? | Emri, T., et al. 2003. J Basic Microbiol. 43: 287-300. PMID: 12872310
- Expression, purification, cristallisation et analyse cristallographique préliminaire d'un domaine RAM autonome à activité hydrolytique de l'hyperthermophile Pyrococcus furiosus. | Agapay, RC., et al. 2005. Acta Crystallogr Sect F Struct Biol Cryst Commun. 61: 914-6. PMID: 16511194
- Purification et caractérisation biochimique de la protéase recombinante du virus de l'immunodéficience simienne et comparaison avec la protéase du virus de l'immunodéficience humaine de type 1. | Grant, SK., et al. 1991. Biochemistry. 30: 8424-34. PMID: 1883829
- Conjugaison du glutathion dans le poumon isolé de lapin perfusé: effets du monoxyde de carbone, de la buthionine sulfoximine et du bleu de cibacron. | Yang, CM. and Carlson, GP. 1990. Toxicol Lett. 52: 47-53. PMID: 2356570
- Site de liaison au glutathion d'une glutathion transférase de classe thêta de bombyx mori. | Hossain, MD., et al. 2014. PLoS One. 9: e97740. PMID: 24848539
- Caractérisation enzymatique de deux glutathion S-transférases de classe epsilon de Spodoptera litura. | Hirowatari, A., et al. 2018. Arch Insect Biochem Physiol. 97: PMID: 29235695
- Cathepsine D des leucocytes humains. Purification par chromatographie d'affinité et propriétés de l'enzyme. | von Clausbruch, UC. and Tschesche, H. 1988. Biol Chem Hoppe Seyler. 369: 683-91. PMID: 3145753
- Conjugaison des substances cancérigènes par les glutathion s-transférases de classe thêta: mécanismes et pertinence pour les variations du risque humain. | Guengerich, FP., et al. 1995. Pharmacogenetics. 5 Spec No: S103-7. PMID: 7581478
- Preuve que la glutathion S-transférase T1-1 humaine de classe Thêta peut catalyser l'activation du dichlorométhane, un carcinogène hépatique et pulmonaire chez la souris. Comparaison de la distribution tissulaire de la GST T1-1 avec celle des classes Alpha, Mu et Pi de la GST chez l'homme. | Sherratt, PJ., et al. 1997. Biochem J. 326 (Pt 3): 837-46. PMID: 9307035
- Caractérisation cinétique de la glutathion transférase T1-1 humaine recombinante, une enzyme de détoxication polymorphe. | Jemth, P. and Mannervik, B. 1997. Arch Biochem Biophys. 348: 247-54. PMID: 9434735
- Régulation de la glutathion S-transférase A5 du rat par des agents chimiopréventifs du cancer: mécanismes de résistance inductible à l'aflatoxine B1. | Hayes, JD., et al. 1998. Chem Biol Interact. 111-112: 51-67. PMID: 9679543
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
1,2-Epoxy-3-(4-nitrophenoxy)propane, 250 mg | sc-258906 | 250 mg | $125.00 | |||
1,2-Epoxy-3-(4-nitrophenoxy)propane, 1 g | sc-258906A | 1 g | $297.00 |
