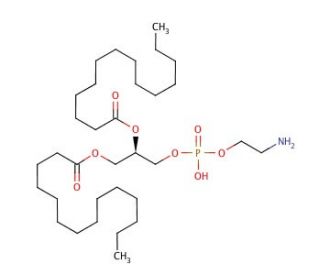
1,2-Dimyristoyl-sn-glycero-3-phosphoethanolamine (CAS 998-07-2)
ACCÈS RAPIDE AUX LIENS
La 1,2-dimyristoyl-sn-glycero-3-phosphoethanolamine, communément appelée DMPE, est un phospholipide synthétique qui joue un rôle essentiel dans l'étude de la biochimie et de la biophysique des membranes. Chaque molécule de DMPE comprend un squelette de glycérol estérifié par deux chaînes d'acide myristique aux positions sn-1 et sn-2, qui sont des acides gras saturés à 14 atomes de carbone. Cette configuration structurelle confère au DMPE la capacité de former des bicouches lipidiques très ordonnées et très serrées, ce qui a un impact significatif sur la fluidité de la bicouche et sur les comportements de transition de phase. La position sn-3 du squelette glycérique est liée à un groupe phosphoéthanolamine, apportant une tête polaire qui confère des propriétés hydrophiles et permet la formation de bicouches stables dans des environnements aqueux. En recherche, le DMPE est largement utilisé pour créer des membranes modèles qui imitent les membranes cellulaires, facilitant l'exploration des interactions lipides-lipides et lipides-protéines, ainsi que la dynamique des processus associés aux membranes. La stabilité et la faible fluidité des bicouches de DMPE les rendent idéales pour étudier les effets de la composition lipidique sur les propriétés des membranes telles que la perméabilité, l'élasticité et les transitions de phase. En outre, l'utilisation du DMPE pour former des liposomes et d'autres systèmes nanostructurés permet aux chercheurs d'étudier les mécanismes d'encapsulation et de libération, ainsi que le rôle des molécules lipidiques dans les voies de signalisation cellulaire et le trafic membranaire, le tout sans impliquer les complexités des systèmes vivants. Grâce à ces applications, le DMPE offre un environnement contrôlé pour disséquer les mécanismes fondamentaux qui régissent la fonction et la dynamique des membranes cellulaires.
1,2-Dimyristoyl-sn-glycero-3-phosphoethanolamine (CAS 998-07-2) Références
- Bicouches planaires de phospholipides utilisés dans la reconstitution de membranes protéiques: étude par microscopie à force atomique. | Doménech, O., et al. 2006. Colloids Surf B Biointerfaces. 47: 102-6. PMID: 16406753
- Les calixarènes dans un environnement membranaire: une étude monocouche sur la miscibilité de trois dérivés p-tert-butylcalix[4]arène bêta-lactame avec la 1,2-dimyristoyl-sn-glycero-3-phosphoethanolamine. | Korchowiec, B., et al. 2007. J Phys Chem B. 111: 13231-42. PMID: 17973515
- La structure des complexes entre la phosphatidyléthanolamine et le glucosylcéramide: une matrice pour les radeaux membranaires. | Quinn, PJ. 2011. Biochim Biophys Acta. 1808: 2894-904. PMID: 21924237
- Effets des pseudopeptides amphiphiles géminés sur les membranes lipidiques modèles: étude de la monocouche de Langmuir. | Rubio-Magnieto, J., et al. 2013. Colloids Surf B Biointerfaces. 102: 659-66. PMID: 23107944
- Effet de la longueur de la chaîne phospholipidique et du groupe de tête sur la formation de la phase bêta du poly(9,9-dioctylfluorène) enfermé dans des liposomes. | Tapia, MJ., et al. 2013. Photochem Photobiol. 89: 1471-8. PMID: 23865822
- Interactions entre les phospholipides et les particules de dioxyde de titane. | Le, QC., et al. 2014. Colloids Surf B Biointerfaces. 123: 150-7. PMID: 25242734
- Étude de mélanges lipidiques binaires d'un lipide cationique à trois chaînes avec des phospholipides adaptés à la diffusion de gènes. | Wölk, C., et al. 2015. Bioconjug Chem. 26: 2461-73. PMID: 26471337
- Sondage des lipides contenant de la phosphoéthanolamine dans les membranes avec la duramycine/cinnamycine et les protéines aegerolysin. | Hullin-Matsuda, F., et al. 2016. Biochimie. 130: 81-90. PMID: 27693589
- Vésicules géantes produites avec des phosphatidylcholines (PC) et des phosphatidyléthanolamines (PE) par des émulsions inversées eau dans huile. | Xu, B., et al. 2021. Life (Basel). 11: PMID: 33801936
- Organisation planaire de l'eau confinée dans les empilements de bicouches lipidiques de phosphatidylcholine et de phosphatidyléthanolamine. | Vancuylenberg, G., et al. 2023. Soft Matter. 19: 5179-5192. PMID: 37279036
- Formation de microdomaines dans les bicouches de phosphatidyléthanolamine détectée par 2H-NMR. | Shin, K., et al. 1995. Chem Phys Lipids. 76: 55-62. PMID: 7788799
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
1,2-Dimyristoyl-sn-glycero-3-phosphoethanolamine, 250 mg | sc-202868A | 250 mg | $204.00 | |||
1,2-Dimyristoyl-sn-glycero-3-phosphoethanolamine, 1 g | sc-202868 | 1 g | $715.00 |
