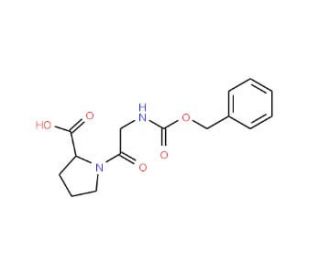
Z-Gly-Pro-OH (CAS 1160-54-9)
ENLACES RÁPIDOS
Z-Gly-Pro-OH es un dipéptido cíclico, que comprende dos aminoácidos unidos por un enlace peptídico. Juega un papel vital en numerosos procesos, atrayendo una atención significativa en la investigación científica. Las aplicaciones de la investigación científica de Z-Gly-Pro-OH han sido diversas e impactantes. Los investigadores lo han utilizado extensamente para adentrarse en las estructuras y funciones de proteínas, péptidos y enzimas. Además, ha sido un activo valioso en el estudio de las membranas celulares y las vías de señalización, desentrañando ideas clave en los procesos celulares. Además, no se puede pasar por alto la contribución de Z-Gly-Pro-OH a la comprensión del ADN, ARN y las vías metabólicas. En cuanto a su mecanismo de acción, aún existen algunas incertidumbres. Sin embargo, se postula que el dipéptido cíclico se une a proteínas y péptidos específicos, desencadenando una cascada de interacciones que regulan procesos celulares vitales. Por ejemplo, se ha observado que se une a ciertas enzimas, facilitando la catálisis de la formación de nuevas moléculas o la descomposición de moléculas existentes.
Z-Gly-Pro-OH (CAS 1160-54-9) Referencias
- El dominio beta-hélice no catalítico de la prolil oligopeptidasa potencia la capacidad catalítica del dominio peptidasa. | Szeltner, Z., et al. 2000. J Biol Chem. 275: 15000-5. PMID: 10747969
- Competencia dependiente del sustrato de la tríada catalítica de la prolil oligopeptidasa. | Szeltner, Z., et al. 2002. J Biol Chem. 277: 44597-605. PMID: 12228249
- Caracterización del sitio activo de una endopeptidasa de escisión post-prolina llamada ZIP, recientemente descubierta y potencialmente importante, mediante LC-UV-MS. | McMahon, G., et al. 2003. Analyst. 128: 670-5. PMID: 12866886
- Análogos del tripéptido neuroprotector Gly-Pro-Glu (GPE): síntesis y relaciones estructura-actividad. | Alonso De Diego, SA., et al. 2005. Bioorg Med Chem Lett. 15: 2279-83. PMID: 15837309
- Propiedades del homólogo de la prolil oligopeptidasa de Pyrococcus furiosus. | Juhász, T., et al. 2006. FEBS Lett. 580: 3493-7. PMID: 16714022
- Cambios conformacionales inducidos por ligandos en la prolil oligopeptidasa: un enfoque cinético. | Van Elzen, R., et al. 2017. Protein Eng Des Sel. 30: 217-224. PMID: 28062644
- Cianación descarboxilativa a temperatura ambiente de ácidos carboxílicos mediante catálisis fotoredox y cianobenziodoxolonas: un mecanismo divergente en comparación con la alquinilación. | Le Vaillant, F., et al. 2017. Chem Sci. 8: 1790-1800. PMID: 28451301
- Colagenasa de Clostridium histolyticum: desarrollo de nuevos sustratos tioéster, fluorogénicos y depsipéptidos y de nuevos inhibidores. | Vencill, CF., et al. 1985. Biochemistry. 24: 3149-57. PMID: 2992578
- Ciclobutilación fotoquímica de radicales centrados en C(sp3) impulsada por tensión-releasa. | Ernouf, G., et al. 2020. Angew Chem Int Ed Engl. 59: 2618-2622. PMID: 31599038
- Estudios de los requisitos de sustrato, propiedades cinéticas e inhibidores competitivos de las enzimas que catabolizan la TRH en el cerebro de rata. | Busby, WH., et al. 1982. Brain Res. 242: 261-70. PMID: 6126250
- Estudios de RMN de un tetrapéptido libre y protegido glycyl-L-prolylglycylglycine en un entorno de soporte beta-turn. | Perly, B., et al. 1983. Biopolymers. 22: 1853-68. PMID: 6616010
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
Z-Gly-Pro-OH, 1 g | sc-296758 | 1 g | $70.00 | |||
Z-Gly-Pro-OH, 5 g | sc-296758A | 5 g | $206.00 |
