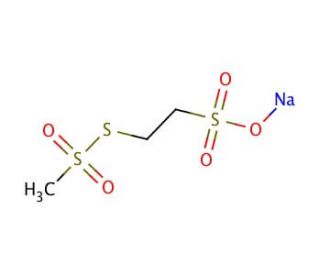
Sodium (2-Sulfonatoethyl)methanethiosulfonate (CAS 184644-83-5)
Ver las publicaciones del producto (1)
ENLACES RÁPIDOS
El (2-Sulfonatoetil)metanosulfonato sódico es una sonda para los canales de los receptores GABAA. Como metanosulfonato, el (2-Sulfonatoetil)metanosulfonato de sodio es sulfhidrilo-reactivo y puede utilizarse para estudiar los residuos de cisteína de las proteínas. El (2-Sulfonatoetil)metanosulfonato sódico reacciona específica y rápidamente con los tioles para formar disulfuros mixtos. El (2-Sulfonatoetil)metanosulfonato sódico sondea las estructuras del canal del receptor ACh del canal del receptor GABAA y de la permeasa de la lactosa. El (2-Sulfonatoetil)metanosulfonato sódico es especialmente eficaz para sondear proteínas nativas asociadas a membranas, como canales y transportadores.
Sodium (2-Sulfonatoethyl)methanethiosulfonate (CAS 184644-83-5) Referencias
1. Dunten, R.L., et al.: Biochem., 32, 3139 (1993),2. Yang, N. et al.: Neuron, 16, 113 (1996),
3. Holmgren, M., et al: Neuropharmacology, 35, 797 (1996),
4. Chahine, M., et al.: Biochem. Bio. Res. Commun., 233, 606 (1997),
5. Ehrlich, B.E., et al.: J. Gen. Physiol., 109, 255 (1997),
6. Lang, R.J., Harvey, J.R., and Mulholland, E.L.Sodium (2-sulfonatoethyl) methanethiosulfonate prevents S-nitroso-L-cysteine activation of Ca2+-activated K+ (BKCa) channels in myocytes of the guinea-pig taenia caeca. Br. J. Pharmacol. 139(6), 1153-1163 (2003).
7. Li, R.A., Tsushima, R.G., Kallen, R.G., et al.Pore residues critical for μ-CTX binding to rat skeletal muscle Na+ channels revealed by cysteine mutagenesis. Biophys. J. 73(4), 1874-1884 (1997).
8. Guan, L., and Kaback, H.R.Site-directed alkylation of cysteine to test solvent accessibility of membrane proteins. Nature Protocols 2(8), 2012-2017 (2007).
9. Engh, A.M., and Maduke, M.Cysteine accessibility in ClC-0 supports conservation of the ClC intracellular vestibule. Journal of General Physiology 125(6), 601-617 (2014).
10. Liu, X., Alexander, C., Serrano, J., et al.Variable reactivity of an engineered cysteine at position 338 in cystic fibrosis transmembrane conductance regulator reflects different chemical states of the thiol. The Journal of Biological Chemisty 281(12), 8275-8285 (2006).
Información sobre pedidos
| Nombre del producto | Número de catálogo | UNIDAD | Precio | CANTIDAD | Favoritos | |
Sodium (2-Sulfonatoethyl)methanethiosulfonate, 250 mg | sc-212933 | 250 mg | $370.00 |
